第一作者简介:包少魁,男,内蒙古兴安盟人,硕士,工程师,研究方向为理化分析。E-mail:baoshaokui@126.com
目的 通过考察基质效应筛选前处理方法,探索一种使用液相色谱-质谱联用法(LC-MS/MS)同时分析血液中氯胺酮和氟胺酮的方法。方法 取1.00mL血液,加入2.00mL乙腈,振荡提取,离心,取上清液过0.22μm滤膜,上样分析。根据保留时间、特征离子对及其丰度比定性,根据特征离子峰面积定量。结果 乙腈沉淀蛋白法基质效应不显著,专属性好,血液中氯胺酮与氟胺酮浓度在1.50~150ng/mL范围内线性较好( R2>0.999),氯胺酮、氟胺酮方法检出限均为0.30ng/mL,不同浓度添加样品回收率在82.1%~86.5%之间,日内、日间RSD均小于10%。结论 本文成功建立了一种液相色谱-质谱联用法同时分析血液中氯胺酮与氟胺酮的方法,该方法操作简便、快捷、灵敏、稳定,适用于血液样品中氯胺酮、氟胺酮的定性定量检验。
Objective To establish a novel method for determination of blood-harbored ketamine and F-ketamine through liquid chromatography-mass spectrometry (LC-MS/MS), with pretreatment choice being preferentially determined from the matrix effect and successively the blood-harbored ketamine and F-ketamine to be isolated and tested of their specificity, linearity, detection limit, precision and accuracy.Methods Sampling blood (1.00mL) was taken, added with 2.00mL acetonitrile, extracted under vibration, and centrifuged, having the supernatant filtered through 0.22μm membrane before analyzed into liquid chromatography-mass spectrometry (LC-MS/MS). With their retention time, characteristic ions and relative abundance ratio for qualitative determination plus their peak area of characteristic ions for quantification, the two chemical substances were to characterize.Results Acetonitrile precipitation showed no significant matrix effect yet good specificity. A good linearity was obtained with the concentration of ketamine and F-ketamine ranging from 1.50ng/mL to 150ng/mL in blood ( R2˃0.999). The detection limit of the method was 0.30ng/mL, and the extraction efficiencies of samples spiked with concentration-different ketamine or F-ketamine were 82.1%~86.5%. The intra- and inter-day RSDs were less than 10%.Conclusions A new method was here successfully developed for determination of blood-harbored ketamine and F-ketamine using liquid chromatography-mass spectrometry (LC-MS/MS). The method is simple, quick, sensitive and stable, suitable for qualitative and quantitative determination of ketamine and F-ketamine in blood.
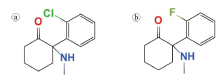
氯胺酮(Ketamine), 即2-(2-氯苯基)-2-甲氨基环己酮, 化学式为C13H16ClNO, 是一种苯环己哌啶衍生麻醉药物[1], 俗称K粉, 为我国典型毒品之一。滥用氯胺酮会使人产生分离性幻觉, 长期滥用会损害泌尿系统、中枢神经系统、心血管系统、呼吸系统、消化系统, 并引发记忆缺失、认知功能损害和精神病[2], 2003年公安部将其列入毒品范畴。随着我国近年来对毒品打击力度的不断加大, 不法分子一直致力于新型毒品的开发, 以便获取经济利益并逃脱法律制裁, 氟胺酮(F-Ketamine)就是其中之一。氟胺酮又名2-(2-氟苯基)-2-甲氨基环己酮, 化学式为C13H16FNO, 其分子结构与氯胺酮的唯一区别就是使用F原子替代了氯胺酮中的Cl原子, 如图1所示, 二者同属苯环己哌啶衍生麻醉药物。王世玉[3]以及Moghimi等[4]均报道过成功合成了氟胺酮, 且发现其具有与氯胺酮相似的麻醉活性, 即滥用氟胺酮一样具有毒品效力。
目前, 氟胺酮在我国多个地区均有缴获, 呈现出越来越严峻的流行趋势, 探索氟胺酮的检验鉴定方法对打击毒品犯罪具有重要实战意义。张磊等[5]和庄顺等[6]相继报道了氟胺酮的气相色谱-质谱(GC-MS)检验方法; Krotulski等[7]和Hä gele等[8]分别使用液相色谱-四级杆飞行时间质谱法(LC-QTOF-MS)和高效液相色谱紫外法(HPLC-UV)检测出了生物检材中的多种新型精神活性物质, 其中包含氟胺酮; Tang等[9]使用液相色谱-质谱法(LC-MS)检出了尿液中的氟胺酮; 谢明清等[10]报道了全血中氟胺酮的高效液相色谱-串联质谱(HPLC-MS/MS)检验方法; 蔡玉刚等[11]也建立了氟胺酮的HPLC-MS/MS检验方法, 并研究了氟胺酮在大鼠体内的代谢规律。鉴于氯胺酮与氟胺酮的结构极其相似, 而且从以往案件总结发现, 吸毒人员所吸食毒品种类往往并不单一, 探究同时对生物检材中氯胺酮与氟胺酮进行定性定量的方法具有重要意义。为丰富苯环己哌啶衍生物的检测手段, 本文就血液中氯胺酮与氟胺酮的液相色谱-质谱联用(LC-MS/MS)检验方法展开相关研究。
Agilent 1260-6420 LC-MS/MS仪器(美国Agi-lent公司), Thermo Biofuge primo离心机(美国Thermo Fisher Scientific公司), TALBOYS 945617涡旋仪(美国TROEMNER), 津腾(尼龙66)0.22 μ m滤膜(天津市津腾实验设备有限公司)。
氯胺酮、氟胺酮标准物质(中国天津阿尔塔科技有限公司, 浓度均为1.00 mg/mL), 甲醇(中国上海MACKLIN)、乙腈(美国J. T. Baker)、甲酸、甲酸铵(美国Fisher Scientific)均为HPLC级, 乙酸乙酯、硼砂为分析纯, 实验用血为取自中心血站的新鲜血液, 实验用水为一级水。
根据需要, 实验用标准溶液均使用甲醇对1.00 mg/mL氯胺酮、氟胺酮标准物质进行逐级稀释得到, 于4 ℃冰箱中保存。
取血液样品1.00 mL置于15 mL塑料离心管中, 加入2.00 mL乙腈沉淀蛋白, 振荡提取10 min, 8 000 r/min离心10 min, 分离有机相, 用0.22 μ m的有机微孔滤膜过滤, 供LC-MS/MS分析。
为与前期研究(LC-MS/MS分析研究毛发中29种毒品)保持延续性, 实验采用LC-MS/MS条件如下:
色谱柱:Kinetex 1.7 μ m Biphenyl 100 Å (LC Column 100 × 2.1 mm); 流动相A:0.01%甲酸-1.0 mmol/L甲酸铵水溶液, 流动相B:乙腈; 进样体积:2 μ L; 流速:0.2 mL/min; 柱温:25 ℃; 洗脱程序见表1。
| 表1 梯度洗脱条件 Table 1 Conditions for gradient elution |
离子化方式:ESI+; 采集模式:多反应监测(MRM), 目标物选择两个母离子/子离子对作为定性离子对, 具体质谱参数及参考保留时间见表2。
| 表2 氯胺酮、氟胺酮的检测参数 Table 2 Mass spectral parameters of ketamine and F-ketamine |
毒物分析中最常用的基质效应评价方法是提取加入法, 通过测定标准溶液的色谱峰面积(S1)和空白样品基质提取液添加标准物质后的色谱峰面积(S2), 以比值S2/S1(%)来评价基质效应。液液萃取和乙腈沉淀蛋白是生物检材中毒物最为常见的提取方法。本文对空白血液按液液萃取法(参考GA/T 1530-2018)和乙腈沉淀蛋白法(文中1.3步骤)处理, 得到空白样品提取液, 空白样品提取液中分别添加氯胺酮、氟胺酮以及氯胺酮和氟胺酮混合标准物质, 使其浓度均为10.0 ng/mL, 得到两种提取方式下的基质添加样品, 按1.4条件检验。取10.0 ng/mL氯胺酮、氟胺酮标准溶液按1.4条件检验, 并计算基质添加样品与标准物质的峰面积比, 计算结果如表3所示。由结果可知, 血液采用液液萃取和乙腈沉淀蛋白两种前处理方法, 基质效应均不显著, 且两种前处理方法中氯胺酮和氟胺酮相互间无明显干扰, 但使用液液萃取法提取血液样品中氯胺酮和氟胺酮的回收率低于乙腈沉淀蛋白法, 且乙腈沉淀蛋白法无需浓缩、复溶等步骤, 操作简单、耗时短, 所需有机溶剂量少, 因此本文后续实验的前处理方法均采用乙腈沉淀蛋白法。
| 表3 两种前处理方法基质效应比较 Table 3 Comparison of matrix effect resulted from two pretreatment choices |
按照1.3操作步骤, 分别对空白血样和空白添加血样(混合添加氯胺酮、氟胺酮浓度为30.0 ng/mL)进行提取, 使用LC-MS/MS测试, 与氯胺酮、氟胺酮标准物质(浓度为10.0 ng/mL)进行比对, 结果显示空白添加血样中氯胺酮、氟胺酮与标准物质保留时间一致, 两特征离子对相对丰度比相似(相对偏差< 10%), 空白血样阴性无干扰, 色谱图见图2。
移取空白血样1.00 mL共7份, 分别添加适量氯胺酮、氟胺酮标准物质, 使血液中氯胺酮、氟胺酮浓度分别为1.50、3.00、6.00、15.0、30.0、60.0、150 ng/mL, 按照1.3操作步骤, 分别进行提取, 供LC-MS/MS分析, 每个样品进样3次, 计算峰面积平均值, 结果如表4所示。
| 表4 氯胺酮、氟胺酮定量离子对峰面积 Table 4 Peak area of quantitative ion pair of ketamine and F-ketamine |
以浓度对定量离子的峰面积进行线性回归, 得到氯胺酮、氟胺酮的线性回归方程分别为:y=60.830x-15.322(R2=0.999 9)、y=96.056x+94.065(R2=0.999 2), 在1.50~150 ng/mL范围内线性关系良好。
于空白血样中添加一组(n=7)低浓度(1.20 ng/mL)的氯胺酮、氟胺酮标准物质, 按照1.3操作步骤, 分别进行提取, 供LC-MS/MS分析, 根据定量结果计算检出限(MDL=t(n-1, 0.99)× S, 其中t(6, 0.99)=3.143, S为7次平行测定的标准偏差), 确定氯胺酮、氟胺酮的方法检出限均为0.30 ng/mL, 以3.3倍检出限作为定量下限, 为1.00 ng/mL。
配制浓度分别为1.50、3.00、6.00、15.0、30.0、60.0、150 ng/mL的氯胺酮、氟胺酮混合标准溶液, 供LC-MS/MS分析, 每个样品进样3次, 计算峰面积平均值, 以浓度对定量离子的峰面积进行线性回归, 得到氯胺酮、氟胺酮的校准曲线, 方程分别为:y=71.565x-10.846(R2=0.999 5)、y=117.603x-10.914(R2=0.999 6)。
使用空白血样配制低中高3个浓度(3.00、15.0、60.0 ng/mL)的氯胺酮、氟胺酮标准物质添加样品, 每一个浓度点平行移取6份, 按照1.3操作步骤, 分别进行提取, 供LC-MS/MS分析, 每一个浓度点每天测定3次, 连续测定3 d, 记录氯胺酮、氟胺酮定量离子对峰面积。使用上述校准曲线回归计算血样中氯胺酮、氟胺酮浓度, 进而计算回收率、日内精密度以及日间精密度, 结果见表5。
| 表5 氯胺酮、氟胺酮的回收率和精密度(n=6) Table 5 Recoveries and precisions of ketamine and F-ketamine (n=6) |
本文成功探索了一种液相色谱-质谱联用法(LC-MS/MS)同时分析血液中氯胺酮与氟胺酮的方法。实验结果表明采用该方法测定血液中的氯胺酮与氟胺酮, 基质效应不显著, 血液中氯胺酮与氟胺酮之间无相互干扰, 专属性好; 血液中氯胺酮与氟胺酮浓度在1.50~150 ng/mL范围内呈现良好的线性关系, 方法检出限为0.30 ng/mL, 定量限为1.00 ng/mL, 精密度以及回收率较高。该方法操作简便, 响应灵敏, 重复性好, 适用于血液中氯胺酮与氟胺酮的定性定量分析, 为苯环己哌啶衍生物的管控及相关案件的检验鉴定提供技术支撑。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|