第一作者简介:吕晨曦,男,山东济宁人,硕士研究生,研究方向为天然药毒物的法医毒物动力学研究。E-mail: 942473823@qq.com
目的 建立超声辅助离子液体-分散液液微萃取-高效液相色谱串联质谱法(high performance liquid chromatography-tandem spectrometry,HPLC-MS/MS)测定全血中卡马西平(carbamazepine,CBZ)的方法。方法 经筛选后以1-丁基-3-甲基咪唑六氟磷酸盐(1-butyl-3-methymidazolium hexafluoro-phosphate, [Bmim][PF6])为萃取剂,在空白血液中添加卡马西平和内标物双氢卡马西平(10,11-dihydrocarbamazepine, CBZ-DiH),通过超声辅助离子液体对其萃取后,采用ZORBAX Eclipse Plus C18 色谱柱分离,流动相A为含0.1%甲酸、10mmol/L乙酸铵的水,流动相B为混合有机溶剂(乙腈‥甲醇=2‥3,体积比),流速1mL/min,采用电喷雾离子源正离子模式(ESI+),多反应监测模式 (MRM) 进行检测。结果 血液中卡马西平的线性范围为8.00 ~ 300.00ng/mL, R2大于0.995,最低检出限为3.00ng/mL,最低定量限为8.00ng/mL,提取回收率大于80%,日内和日间精密度均小于20%。采用本方法从实际案件的血液样品中检出卡马西平,浓度为2.71µg/mL。结论 本研究建立的全血中卡马西平的检测方法,具有环境友好、快速、富集效果好、灵敏度高、有机溶剂消耗小的优点,可应用于卡马西平相关案件的法医学鉴定。
Objective To establish a novel approach of determining carbamazepine in whole blood through ultrasonic-assisted ionic liquid dispersive liquid-liquid microextraction coupled with HPLC-MS/MS (high performance liquid chromatography-tandem spectrometry).Methods With the selected 1-butyl-3-methylimidazolium hexafluoro-phosphate ([Bmim][PF6]) as extract solvent and 10,11-dihydrocarbamazepine as internal standard, the blank whole blood samples were added of carbamazepine, subjected to treating with ultrasound-assisted ionic liquid dispersive liquid-liquid microextraction. The harvested extraction was consecutively separated with ZORBAX Eclipse Plus C18 column that was flowed with mobile phases [A: 0.1% formic acid aqueous solution plus 10mM ammonium acetate and B: acetonitrile/methanol (v/v, 2:3)] running at the rate of 1mL/min. The detection was chosen under the mode of ESI+ plus MRM (multiple reaction monitoring).Results Carbamazepine was of linearity with it ranging from 8.00ng/mL to 300.00ng/mL in whole blood, with its correlation coefficient ( R2) greater than 0.995, limit of detection (LOD) being 3.00ng/mL and limit of quantification (LOQ) 8.00ng/mL. The here-established approach was of extraction recovery greater than 80%, intra- and inter-day precision (relative standard deviation, RSD) being both less than 20%. Through verification of the here-established approach, a real forensic case was identified with carbamazepine of 2.71μg/mL in the victim's whole blood.Conclusions The here-developed approach is environmentally friendly, rapid, of good enrichment effect, high sensitivity and low consumption of organic solvent, capable of being used for determination of carbamazepine in biological samples from related forensic poisoning cases.
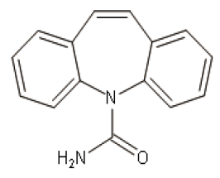
卡马西平(carbamazepine)亦称酰胺咪嗪, 化学结构类似三环类抗抑郁药, 化学结构式见图1。卡马西平对控制癫痫大发作、精神运动性发作、局限性发作和混合型癫痫均有效, 其中对精神运动性发作疗效最好, 为目前的首选药, 也用于缓解三叉神经痛、舌咽神经痛和外伤性神经痛等[1]。在临床治疗中, 癫痫和神经痛患者需要长期使用本品, 致使其用药依从性降低, 过量用药导致中毒或者死亡的案例也时有发生[2]。因此, 对临床样本和中毒案件检材中卡马西平含量的及时检测尤为重要, 不仅可以为临床治疗的规范用药提供依据, 也可为中毒案件的侦破提供科学的依据。
目前卡马西平血药浓度的检测方法主要有液相色谱法、液相色谱质谱法和气相色谱质谱等方法, 但采用超声辅助离子液体-分散液液微萃取-液相色谱质谱联用法尚未见报道。据文献报道生物检材中卡马西平的前处理常使用液液萃取或固相萃取[3, 4, 5], 液液萃取法检材用量较大、提取过程较为繁琐费时, 需要使用大量有机溶剂作为萃取剂, 从而导致环境污染; 固相萃取所需的检测成本比较高, 且操作过程复杂。近年来, 离子液体作为一种新型的样品萃取剂可以有效克服以上缺点, 且它具有蒸气压低、液态范围宽、环境友好等优势, 被越来越广泛地应用到样品前处理中[6, 7]。基于离子液体在样品前处理中的优势, 本研究建立了一种高效快速、便捷、有机溶剂用量少的超声辅助离子液体-分散液液微萃取-液相色谱质谱联用检测血液中卡马西平的方法。
1260-6470液相色谱-三重四级杆串联质谱仪(美国Agilen公司), Neofuge 15R 高速低温离心机(上海力申科学仪器有限公司), 20、100 μL和1 mL的移液器(德国Eppendorf公司), Milli-Q超纯水系统(德国Merck Millipore公司), BP211D精密电子天平(德国Sartorious公司)。
空白血液样本(来自于健康家兔, 山西医科大学动物中心提供); 卡马西平(纯度≥ 98%, 加拿大 TRC公司)、双氢卡马西平(纯度为99%, 美国TargetMol公司); 乙腈、甲醇(色谱级, 中国 Sigma-Aldich公司); 1-丁基-3-甲基咪唑六氟磷酸盐([Bmim][PF6])、1-己基-3-甲基咪唑六氟磷酸盐([Hmim][PF6])和1-辛基-3-甲基咪唑六氟磷酸盐([Omim][PF6])纯度均为99%, 均来自中科院兰州物理化学研究所; 盐酸(37%, 天津科密欧公司)、丙酮(分析纯, 天津科密欧公司); 氢氧化钠(97%, 天津大茂公司); 甲酸(色谱级)、乙酸铵(≥ 99.0%)均购自上海阿拉丁生化科技股份有限公司; 氯化钠(≥ 99.5%, 天津市大茂化学试剂厂)。
分别精确称量10.0 mg的卡马西平、双氢卡马西平标准品于两个10 mL容量瓶中, 用甲醇定容至刻度, 得到1 mg/mL的标准工作液, -20 ℃储存, 备用。
精密量取待测血液样品100 μL置于1.5 mL聚四氟乙烯尖底离心管中, 依次加入50 μL的卡马西平标准品溶液(3.2 μg/mL)、50 μL内标双氢卡马西平溶液(1 μg/ mL), 再加入800 μL超纯水、40 μL 9%氯化钠溶液和20 μL10%氢氧化钠溶液。将60 μL萃取剂[Bmim][PF6]加入其中, 最后加入300 μL分散剂丙酮, 涡旋振荡20 s, 超声提取20 min, 置于4 ℃ 冷冻离心机中以5 000 r/min离心5 min, 然后将100 μL移液器轻轻插入下层离子液体中央, 吸取30 μL的下层液体置于另一1.5 mL离心管中, 经甲醇稀释10倍后, 过0.22 μ m有机膜, 2 μL进样, 供LC-MS/MS检测。
1)色谱条件。色谱柱:ZORBAX Eclipse Plus C18 column (4.6 mm×150 mm, 5 μ m); 流动相A:水(含0.1%的甲酸、10 mmol/L的乙酸铵), 流动相B:混合有机相(乙腈:甲醇=2:3, 体积比); 梯度洗脱:流动相B初始比例45%保持6 min, 7 min内升至100%保持2 min, 9~11 min内降至45%后保持2 min, 流速1 mL/min, 进样量2 μL。
2)质谱条件。电喷雾离子源(ESI), 正离子模式, 多反应监测(MRM)扫描模式; 雾化干燥气温度:300 ℃; 气流速:5 L/min。待测物质谱参数见表1。
| 表1 卡马西平、双氢卡马西平的质谱参数 Table 1 Mass spectrometric parameters of CBZ and CBZ-DiH |
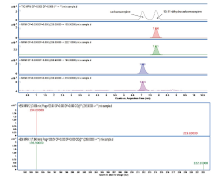
卡马西平和内标双氢卡马西平在上述1.4检测方法下, 色谱行为良好, 保留时间分别是7.068和7.833 min, MRM色谱图和质谱图见图2。
方法学验证主要参考相关规范和文献[8, 9], 包括线性、检出限和定量限、精密度(日内和日间)、准确度、提取回收率、基质效应和稳定性。
2.2.1 线性范围、检出限和定量限
将卡马西平标准液加入100 μL空白血液中, 配制成浓度为8、50、100、150、200、250、300 ng/mL的加标样本, 每个浓度平行制样3次, 按照1.3方法进行样品前处理, 1.4仪器条件进行样品分析检测, 得到的线性方程权重为1/x, 用R2对线性进行评估, 方法检出限(LOD, S/N=3)和定量限(LQD, S/N=10)见表2。
| 表2 卡马西平在血液中的线性范围、检出限和定量限 Table 2 The linear equation, LOD and LQD of CBZ in blood |
2.2.2 精密度和准确度
本研究中添加三个浓度为16.00 ng/mL(线性最低浓度的2倍)、80.00 ng/mL(线性最低浓度的10倍)和240.00 ng/mL(线性最高浓度的80%)质控样本。每个浓度配制5个平行样本, 共15个平行样本, 一日之内分早、中、晚三次进样得到日内精密度。每个浓度配制15个平行样本, 每天取出5个平行样本, 相应时间段内连续测3 d, 得到日间精密度。每个浓度配制5个平行样本, 一次进样得到准确度, 结果见表3。
| 表3 卡马西平在血中的精密度和准确度 Table 3 Accuracy and precision of CBZ in blood |
2.2.3 提取回收率、基质效应和稳定性
选低、高两个质控浓度进行空白添加, 每个浓度平行5次, 按照上述1.3方法进行样本提取。先取10个空白基质样本, 按上述方法进行提取, 在最后的提取液中加入标准液, 配制低和高两个浓度样本。配制的低和高两浓度的甲醇稀释液, 用上述1.4分析方法对以上所有样本进行同批次检测, 得到提取回收率和基质效应, 结果见表4。分别考察低和高两个质控浓度的样本, 每个浓度各平行5次, 24 h之内在室温下放置3 h而后在-80 ℃放置21 h, 重复三个循环, 然后进行仪器分析测定, 稳定性结果见表4。
| 表4 卡马西平在血液中的提取回收率、基质效应和稳定性 Table 4 Recovery, matrix effect and stability of CBZ in blood |
为提高方法的提取效率, 本研究从离子液体种类和体积、分散剂种类和体积、pH值、盐浓度、超声时间和与传统提取方法比较6个方面进行讨论。根据文献报道, 选用峰面积作为优化的评估参数[10, 11]。
为了筛选出一种合适的离子液体, 需要考虑如下几个因素:密度要比水大、疏水性强、常温下要保持液态[12]。综合以上因素和研究结果, 从[Bmim][PF6]、[Hmim][PF6]和[Omim][PF6]三种离子液体中筛选出[Bmim][PF6]为最适萃取剂。另外, 离子液体体积也是重要影响因素, 本研究依次将40 、60、80、100 μL的[Bmim][PF6]离子液体分别加入到萃取体系中, 经过振荡、超声和离心后分别定量回收10、30、40、50 μL离子液体进行检测, 最终选出离子液体体积60 μL为最佳。结果见图3。
本研究选择三种分散剂:甲醇、乙腈和丙酮, 分别加入提取体系中, 发现丙酮的提取效果最好。此外又进一步探究了分散剂体积这一因素, 分别加入体积为150、200、250、300 μL的丙酮进行优化, 得出最优的分散剂体积为300 μL。结果见图4。
为探究提取体系的酸碱度对提取效果的影响, 调节提取体系pH分别为3、5、9和11及不添加酸碱(等效加入超纯水), 发现当pH=9时提取效果最好, 结果见图5。
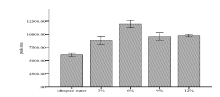
考察在提取体系中分别加入超纯水、3%、6%、9%和12%的氯化钠溶液对提取效率的影响。发现当盐浓度为6%时体系萃取效率最高(图6)。原因可能是卡马西平在不同盐浓度下盐析效应和静电作用所占的主导地位不同导致体系对待测物的提取效率不同[13]。
胡某, 男, 40岁, 于2017年7月30日晚11时50分死亡, 据家属称死者有癫痫史。解剖后, 提取血样送检。将本案中的血样(-20 ℃保存)依据本研究建立的方法检测, 随行标准曲线定量, 从送检的死者血液中检出卡马西平, 浓度为2.71 μg/mL。对于检血中浓度进行了稀释效应讨论, 具体操作如下:
在空白血液中添加卡马西平浓度2.70 μg/mL, 稀释10倍, 制得6个平行样本。同时建立卡马西平浓度依次为8、50、100、150、200、250、300 ng/mL的加标工作曲线, 依据本研究中样品前处理过程和本研究中建立的方法检测, 将制得6个平行样本, 依据所建立的随行工作曲线进行测定, 曲线方程为y=1.131 647x+0.004 013, R2=0.993 3, 6个样本浓度分别为247.49、248.50、243.54、251.78、248.82、253.28 ng/mL, 测得的平均浓度为 (249.07±3.42) ng/mL, 与理论稀释值270.00 ng/mL相比, 平均稀释结果为92.25%, 在85%~115%范围之间[16], 说明在稀释的情况下, 使用本方法进行定量分析依旧具有较高准确性和可靠性。
本研究将绿色的离子液体作为萃取溶剂代替有毒性且挥发性强的有机溶剂, 建立了超声辅助离子液体-分散液液微萃取-高效液相色谱串联质谱法测定全血中卡马西平的新方法。本研究建立的方法不仅可以为临床药物浓度监测提供科学依据, 同时也可以为卡马西平相关法医学中毒案件的检测提供技术支持。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|