第一作者简介:徐琛,男,浙江杭州人,硕士,工程师,研究方向为法医毒物分析。E-mail: o7o81985@163.com
目的 建立血液中4类(7种)鼠药(毒鼠强、氟乙酸根、溴敌隆、大隆、杀鼠灵、杀鼠醚、氟鼠灵)的超高效液相色谱-高分辨质谱(UPLC-HRMS)快速检测方法。方法 采用乙腈为蛋白沉淀剂,用PLD+净化柱或有机微孔过滤膜净化提取液,用UPLC-HRMS对血液中的4类(7种)鼠药进行定性定量检测。分析采用Luna Omega PS C18(2.1mm×100mm, 3µm)色谱柱,质谱扫描方式为负离子的全扫描/实时二级质谱扫描(Full MS/ddMS2)模式,一级全扫描( m/ z 50~750)分辨率为 70000,二级扫描(ddMS2)分辨率为17500。结果 毒鼠强、氟乙酸根、溴敌隆、大隆、杀鼠灵、杀鼠醚、氟鼠灵的检出限均为50ng/mL,3个添加水平下的回收率为85.3%~94.7% ,日内相对标准偏差(RSD)为3.4%~11%( n=6),日间相对标准偏差(RSD)为5.6%~13% ( n=6)。结论 使用本方法可同时准确测定血液中的4类(7种)鼠药。
Objective To develop an analytical method for simultaneous determination of seven rodenticides (TETS, fluoroacetic acid, bromadiolone, brodifacoum, warfarin, coumatetralyl and flocoumafen) (categorized into 4 major kinds) in whole blood through ultra-high performance liquid chromatography-high resolution mass spectrometry (UPLC-HRMS).Methods The samples were treated with acetonitrile to precipitate protein, successively extracted through purification of PLD+ polymer column or organic microporous filter membrane. Luna Omega PS C18 chromatographic column (2.1mm×100mm, 3µm) was adopted for chromatographic separation with gradient elution. The analytes were detected under the mode of negative-ion ESI in full MS/ddMS2.Results Detection limits (LODs) of the seven rodenticides varied among 10~50 ng/mL. The recoveries ranged from 85.3%~94.7% at three spiked levels in whole blood. The intra-day relative standard deviation (RSD) was 3.4%~11% ( n=6), with the inter-day’s being 5.6%~13% ( n=6).Conclusion This method is both qualitative and quantitative, capable of simultaneous and accurate screening of seven rodenticides in whole blood.
鼠药分为急性杀鼠药和慢性杀鼠药。急性杀鼠药有毒鼠强、氟乙酰胺、氟乙酸钠、鼠立死、鼠特灵、灭鼠优等品种, 其中毒鼠强、氟乙酰胺、氟乙酸钠由于其见效快, 灭鼠效果好等特点曾在我国广泛使用, 但因其毒性大、易引起二次中毒等原因也造成大量人畜伤亡, 现已被国家明令禁用。目前应用最广的是慢性抗凝血类杀鼠药, 具有高效灭鼠、对人畜毒性低, 且有特效解毒药等特点[1]。抗凝血类杀鼠药是由4-羟基香豆素类(杀鼠灵、杀鼠醚、鼠得克、大隆、溴敌隆、氯灭鼠灵、噻鼠灵、氟鼠灵、敌鼠灵、克灭鼠)和茚满二酮类(敌鼠、氯敌鼠)衍生而来的一类杀鼠药。毒鼠强和氟乙酸类鼠药虽已禁止生产, 但在偏远地区仍有遗留[2]。目前广泛使用的慢性鼠药由于使用不当也经常引起人和牲畜中毒[3], 两类鼠药也时常被犯罪分子用来投毒, 给人民的生命安全带来威胁。因此研究建立一种快速筛查血液中多种常见鼠药的方法具有重要意义。
氟乙酸钠、氟乙酰胺进入生物体内代谢为氟乙酸, 由于氟乙酸为小分子且极性大、易溶于水, 之前采用的气相色谱法[4, 5]、气相色谱-质谱联用法[6, 7], 液相色谱-串联质谱法[8, 9]等都需要较复杂的前处理过程; 毒鼠强检测多采用气相色谱-质谱联用法; 抗凝血类鼠药检测目前最便捷的方法是液相色谱-串联质谱法, 可一次性筛查多种抗凝血类鼠药[10]。
在公共安全领域, 疑似鼠药中毒事件发生后, 必须第一时间确定毒物种类、明确事件性质, 为之后的案(事)件调查提供技术支撑。而目前针对不同类型鼠药需要采取不同的前处理、检验方法, 满足不了时效性的要求。本研究基于实际案件的法医毒物检测需求[11, 12], 对4类(7种)不同性质的鼠药采用同一种前处理方法, 应用超高效液相色谱-高分辨质谱法(UPLC-HRMS)进行快速定性定量筛查。
Q-Exactive四级杆-静电场轨道阱高分辨质谱(美国ThermoFisher Scientific), Ultimate 3000超高效液相色谱系统(美国DIONEX 公司), 5430R离心机(德国EPPENDORF公司), VORTEX-5涡旋混合器(海门其林贝尔公司), 微量移液器(德国EPPENDORF公司)。PLD+净化柱(瑞典Biotage公司)。
毒鼠强、氟乙酸钠标准品购自公安部物证鉴定中心, 溴敌隆、大隆、杀鼠灵、杀鼠醚和氟鼠灵标准物质均购自上海安谱科学仪器有限公司。
甲醇(HPLC级); 甲酸(HPLC级); 乙腈(HPLC级); 去离子水(二级水); 空白血液由近期未服用任何药物的健康志愿者提供。
根据毒鼠强、氟乙酸根、溴敌隆、大隆、杀鼠灵、杀鼠醚和氟鼠灵标准物质的纯度和盐型换算, 各称取适量标准物质, 用甲醇分别配制成1.0 mg/mL毒鼠强、氟乙酸根、溴敌隆、大隆、杀鼠灵、杀鼠醚和氟鼠灵标准物质储备溶液, 4 ℃避光密封保存, 有效期6 个月。分别取7种鼠药的标准物质储备溶液适量, 用甲醇配制成7种鼠药含量均为10 μ g/mL混合标准工作溶液, 有效期3个月。实验中所用其他浓度的单一标准工作溶液均由1.0 mg/mL标准物质储备溶液配制得到。
移取全血样品1.0 mL于具盖离心管中混匀。加入乙腈3 mL, 振荡5 min, 不低于8 000 r/min离心10 min, 取上清液, 置于浓缩器上60 ℃浓缩至干, 加入初始流动相0.5 mL定容, 经有机微孔滤膜或净化柱过滤(取上清液转移至净化柱中, 控制上清液过柱流速不超过5 mL/min, 收集洗脱液)作为检材提取液, 供仪器检测。
1.4.1 色谱条件
色谱柱:Luna Omega PS C18(2.1 mm× 100 mm, 3 µ m); 柱温:40 ℃; 流速:0.4 mL/min; 进样量:5 µ L; 流动相A:0.1%甲酸水溶液; 流动相B:含0.1%甲酸乙腈; 梯度洗脱程序:0~1.5 min, 95% A; 1.5~5.0 min, 95%~5%A; 5.0~8.5 min, 5% A; 8.5~8.6 min, 5%~95% A; 8.6~10. 0min, 95% A。
1.4.2 质谱条件
离子源:电喷雾离子源(HESI); 质谱扫描方式为负离子的全扫描/实时二级质谱扫描(Full MS/ddMS2)模式, 一级全扫描(m/z 50~750)分辨率为 70 000, 二级扫描(ddMS2)分辨率为17 500。MS/MS模式时, 所用碰撞能为阶梯能量为30、40和50 eV。鞘气:40 Arb; 辅助气:10 Arb; 喷雾电压:3 000 V; 离子传输管温度:320 ℃; 辅助气温度:100 ℃; 离子源温度:450 ℃。7种鼠药的质谱特征离子见表1。
| 表1 七种鼠药的质谱特征离子 Table 1 Mass spectrometric characteristic ions of seven rodenticides |
取6份不同来源不含检测药物的空白全血, 将定性量下限浓度的7种鼠药加入到空白全血中, 按1.3方法进行样品处理, 按1.4的色谱和质谱条件进行分析, 得到7种鼠药的色谱图与高分辨质谱图(图1)。
结果表明该方法可将7种鼠药较好地进行分离, 药物相互之间不影响测定。
取空白全血样品混合标准工作溶液, 配制成浓度为50、100、200、400、800 ng/mL的样品。按1.3和1.4方法进行样品处理和分析, 以各被测物浓度为横坐标, 以被测物峰面积为纵坐标, 进行加权(W=1/x)最小二乘法回归运算, 得回归方程、相关系数、线性范围。结果表明7种鼠药在50~800 ng/mL浓度范围内均线性关系良好(R=0.993 2~0.998 5)。以色谱信号S/N=3的药物浓度为检出限, 血液中毒鼠强检出限为50 ng/mL, 氟乙酸根检出限为50 ng/mL, 溴敌隆、大隆、杀鼠灵、杀鼠醚、氟鼠灵检出限为10 ng/mL。
取空白全血样品, 添加不同量的混合标准工作溶液, 配制成50、200、800 ng/mL 3个浓度的质控样品, 按1.3和1.4方法进行样品处理和分析, 每一浓度进行6样本分析, 测试3 d, 计算准确度、日内精密度、日间精密度。结果表明准确度为85.3%~94.7%; 日内精密度(RSD)为3.4%~11%; 日间精密度(RSD)为5.6%~13%。
采用提取后添加法, 同时考察绝对基质效应和提取回收率。方法如下:取空白全血, 配制50、200、800 ng/mL 3个浓度的血液样品, 每一浓度进行6样本分析, 按1.3方法进行样品处理, 得各待测物峰面积Ax。另取相应浓度的标准溶液, 吹干, 复溶, 分析得各待测物峰面积As。同时取空白全血样品, 直接按1.3方法进行处理, 然后向获得的有机相中加入相应浓度的标准溶液, 再按1.3方法吹干, 复溶, 分析得各待测物峰面积Am。提取回收率=Ax/As× 100%。绝对基质效应=Am/Ax× 100%。另外选取6份不同来源的空白全血样品, 计算不同来源绝对基质效应的相对标准偏差(RSD), 获得相对基质效应。结果表明7种鼠药的提取回收率为84.1%~95.9%, 绝对基质效应为87.5%~104.6%, 相对基质效应为4.7%~8.7%。
本试验考察了空白添加全血样品在室温下放置1 d、4 ℃避光条件下放置3 d以及储备液在4 ℃避光条件下放置180 d的稳定性。每一种稳定性考察50、200、800 ng/mL三个浓度, 每个浓度进行5样本分析。结果表明空白添加全血样品在室温下放置1 d稳定, 相对误差(RE)=5.3%~9.7%; 在4℃避光条件下放置3 d稳定, RE=6.2%~12%; 储备液在4℃避光条件下放置180 d稳定, RE=2.5%~4.9%。
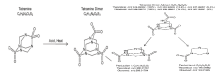
7种鼠药的质谱条件优化过程中, 除毒鼠强外的其余6种鼠药离子化方式相对常规, 前体离子和二级特征离子较易确定。而毒鼠强离子化过程特殊, 其原理经过反复实验, 确认如下:采用Q-Exactive四级杆-静电场轨道阱高分辨质谱对毒鼠强进行检测, 得到一级质谱图(图2左)和二级质谱图(图2右)。软件根据同位素比例计算得出毒鼠强的前体离子和二级特征离子的分子式分别C5H11O6N6S3、C5H10O4N5S2和C3H6O2N3S。
此实验结果与Owens 等[13]所述的毒鼠强聚合、裂解过程(图3)相吻合, 符合化学原理。
由于鼠药种类较多、性质各异, 本实验尝试了固相萃取、乙酸乙酯液液提取、乙腈蛋白沉淀三种提取方式。其中固相萃取和液液提取法均无法提取出氟乙酸根, 只有蛋白沉淀法可以同时提取7种药物, 而且操作简便、成本低, 通用性好, 除可同时提取血液中4类鼠药外, 还可提取法医毒物领域中其他大多数目标药物, 在实际办案中有十分重要的意义, 故选择其作为前处理方法。
由于毒鼠强的离子化需要在酸性反应下进行, 故考察了2种色谱条件, 分别为在流动相A和B中均加入甲酸、乙酸, 在不同条件下观察色谱峰峰形。观察发现, 加入乙酸时氟乙酸根离子化被严重抑制, 响应强度不理想, 而当流动相A和B中各加0.1%甲酸时, 能同时保证4类鼠药均获得较好的响应强度, 分离度好、峰形尖锐。故选择A:0.1%甲酸水溶液、B:含0.1%甲酸乙腈作为流动相。
比较PFP、C18、PS C18三种填料的色谱柱的分离效果, 发现C18色谱柱中氟乙酸根无保留, PFP色谱柱中抗凝血类鼠药的分离效果差。只有PS C18色谱柱能兼顾4类鼠药的检测。
2019年, 杭州淳安市马某因长期牙龈出血就医, 应用此方法进行检测, 2 h内就确定了此人为大隆中毒, 帮助医院快速确定医疗策略。后续对马某家中食材进行检验, 在食用油中检出大隆, 很快确定了嫌疑人, 防止受害人的伤害进一步扩大。
本研究建立的UPLC-HRMS检测方法能够同时检测全血中4类(7种)鼠药(毒鼠强、氟乙酸根、溴敌隆、大隆、杀鼠灵、杀鼠醚和氟鼠灵)。本方法基质干扰小, 操作简单, 可进行日常疑似鼠药投毒案件的筛查, 能够满足日常办案的需要。此外本方法也具有很好的兼容性, 可改进质谱参数, 如采用正负离子同时扫描后, 可筛查更多药物。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|