第一作者简介:乐浩鸣,男,四川西昌人,学士,工程师,研究方向为刑事理化检验和毒品检验。E-mail: brad830331@126.com
目的 建立测定涉毒人员毛发样本中硝甲西泮的液相色谱-质谱/质谱(HPLC-MS/MS)分析方法。方法 对质谱主要参数进行优化,采用电喷雾多反应监测模式(MRM)测定不同浓度标准样品并建立标准曲线,通过准确度、灵敏度和实际案例检材的检验对方法进行评价。结果 标准溶液最低检出限0.1ng/mL,线性范围宽, R2 >0.999,空白毛发外添加标样回收率>80%。结论 优化后的毛发样本中硝甲西泮的HPLC-MS/MS操作简便快捷,灵敏度高,重现性好,具备定性定量的适用性和可靠性。
Objective To develop a HPLC-MS/MS method for identifying the nimetazepam in human hair sampled from drugger.Methods The sampling hair was cleaned and then ground into powder that was spiked (for the blank sample) or extracted (for the drugger’s) of nimetazepam, with the received solution potentially containing nimetazepam subjected to HPLC-MS/MS analysis whose main mass spectrometric parameters were previously optimized. The standard samples were determined through electrospray plus multiple reaction monitoring (MRM) so that the standard curve was established. The method was evaluated from the items of accuracy and sensitivity, having been verified with the samples of actual cases.Results The standard solution was of minimum detection limit as 0.1ng/mL, showing wide linear range and the coefficient of determination being R2>0.999. The standard sample recovery rate was >80% for the blank hair. Positive result of nimetazepam was obtained from the samples of actual case.Conclusion HPLC-MS/MS is simple, sensitive and reproducible, demonstrating its applicability and reliability for qualitative and quantitative detection of nimetazepam.
硝甲西泮(Nimetazepam)是一种具有中枢神经抑制作用的精神药物, 原为治疗焦虑、失眠等症状的医疗管制药品, 可用于合成苯二氮卓类新型策划药[1], 俗称“ 一粒眠” “ K5” “ 红5” “ 开心佛” , 近年来在地下夜场和慢摇吧比较风行, 多为“ 摇头族” 用来“ 解High” 的情绪舒缓剂, 有毒贩误导青少年将其作为可待因类糖浆的替代品使用, 在警方临检采尿时避免被检测出滥用药品。因其见效快, 也是犯罪分子实施麻醉抢劫的主要选择药物。
目前硝甲西泮类检验报道较多的为缴获可疑样品的气质联用仪检验[2], 以及血液中一般苯二氮卓类安眠镇静药物的HPLC-MS/MS检验[3], 生物样品如人体血液、尿液、毛发中残留硝甲西泮的液质联用仪检验方法报道较少。因液质联用仪的MRM模式可获得更高的检测灵敏度, 更适用于生物样品中痕量药物的检测[4, 5, 6]。本实验室建立了涉毒人员毛发样本中硝甲西泮的HPLC-MS/MS分析方法, 具备操作简便快捷、灵敏度高、重现性好等特点, 为该类药物滥用者的毛发等生物样本检验提供参考和帮助。
Agilent 1290 Infinity Ⅱ 液相色谱系统, 配备 G7120A 型二元泵、G7167B 型自动液体进样器、G7116B 型柱温箱; Agilent 6470 三重四极杆液质联用系统; 万孚毒品检测仪(北京万孚); METTLER TOLEDO 电子天平; 移液器, 高速离心机(THERMO); Agilent Captiva Nylon 0.2 μ m 滤膜及各种常规一次性实验器具。
硝甲西泮标准物质(美国SIGMA公司), 用甲醇配制浓度为1 mg/mL标准储备液, 于4 ℃下冷藏保存。
乙酸铵、磷酸三钾(天津科密欧, 色谱纯); 异丙醇、丙酮、二氯甲烷(四川西陇科技, 分析纯), SDS(天津佰伦斯, 分析纯); 氨水、盐酸(成都金山化学试剂, 分析纯)。
乙腈、甲酸、甲醇均为质谱纯, 购自 Merck公司; 纯水由 Milli-Q 超纯水系统制得。
1.2.1 液相色谱条件
色谱柱:Agilent ZORBAX Eclipse Plus-C18 色谱柱 (2.1 mm× 50 mm× 1.8 μ m); 柱温:40 ℃, 进样体积:1 μ L。流动相A:0.1%乙酸+5 mmol/L乙酸铵水溶液; 流动相B:甲醇; 运行时间:18 min; 流速:0.2 mL/min。梯度洗脱程序见表1。
| 表1 梯度洗脱条件 Table 1 Gradient elution conditions |
1.2.2 质谱条件
ESI正离子模式; 鞘气温度:300 ℃; 鞘气流速:12 L/min; 干燥气温度:300 ℃; 干燥气流速:10 L/min; 雾化器压力:45 psi; 毛细管电压:+4000 V/-3500 V; 喷嘴电压:+500 V; Delta EMV:+300 V/-500 V。
取1 mg/mL硝甲西泮标准储备液分别用流动相稀释配成0.1、 1、10、 50、100 ng/mL梯级浓度的标准工作溶液, 当天配制。取志愿者提供的空白毛发样本3份各50 mg, 分别用SDS、丙酮和水清洗后, 置研磨管中(含撞珠), 添加硝甲西泮标准品(添加浓度按低、中、高分别为0.01、0.1、1.0 μ g/mL), 加入溶解液湿法高速研磨处理[7], 取液体, 过0.22 μ m水相膜, 供LC-MS/MS分析。另取志愿者提供的空白毛发样本3份各60 mg在浓度分别为100、10、1 μ g/mL硝甲西泮标准溶液中浸泡(只能模拟药物经汗腺分泌及被动污染进入毛发的方式, 不能模拟经血液循环的进入方式[8]), 按1、3、7 d的浸泡时间分别取每份的三分之一(约20 mg)作为实验样本, 经相同程序清洗洗涤、晾干, 提取后供LC-MS/MS分析。
为获得最佳分析结果, 保证目标物定性定量的准确性, 对待测物的质谱检测参数碎裂电压和碰撞能量进行了优化, 优化后的目标物硝甲西泮MRM质谱条件见表2。
| 表2 优化后的目标物硝甲西泮MRM质谱条件 Table 2 Optimized MRM mass spectral conditions of the targeted compound, nimetazepam |
在流动相选择上, 因A相加入乙酸铵, 若B相使用乙腈, 在偏酸性环境下乙腈含量超过70%时可能发生不互溶, 因此B相使用甲醇, 并降低乙酸铵浓度, 选取3个浓度进行优化, 发现5 mmol/L乙酸铵浓度能得到最高的乙酸铵响应, 高于此浓度目标位出峰时间延后且响应值降低。另实验考查了从2 min起和4 min起梯度缓慢升高对峰形的影响, 从2 min起梯度缓慢升高峰形对称, 而4 min起缓慢升高B相梯度会产生一定拖尾。
在优化后的仪器最佳工作条件下将1.3中不同浓度标准工作液同空白对照一起分别进样, 通过MRM模式以被测组分峰面积为纵坐标, 浓度为横坐标, 绘制标准工作曲线, 数据用线性最小二乘回归曲线进行拟合, 权重为1/x, 不强制过原点。得到线性回归方程y=9.143x+18.3(R2=0.9999); 表明硝甲西泮于浓度范围0.1~100 ng/mL内线性关系良好。
方法检出限通过逐次减少样本中含有目标物的毛发数量分析计算, 即取一定量已知阳性样本与空白毛发混合, 以此稀释, 取50 mg平行操作进样后根据标准曲线计算浓度, 以3倍信噪比响应且保留时间偏差在0.2以内的样品浓度为检出限(LOD), 以信噪比不小于10且保留时间偏差在0.2以内浓度为定量限(LOQ), 浓度计算结果0.025 ng/mg样品的SNR=3.7, 浓度计算结果0.1 ng/mg样品的SNR=10.7, 因此该方法中硝甲西泮检出限为0.025 ng/mg, 定量限为0.1 ng/mg。
在空白毛发样本中添加硝甲西泮标准品, 分高、中、低添加浓度分别为0.01、 0.1、1 μ g/mL样品, 如1.3中样品处理方法, 进行加标回收率实验(因添加样品只是同空白毛发混合而未进入毛发内, 该回收率只能代表前处理过程药物损失率, 而不反映实际阳性毛发样本的提取情况), 每一浓度平行6样。结果0.01、0.1、1 μ g/mL3个浓度的平均回收率分别为92.4%、80.7%、75.9%, RSD分别为6.83%、2.55%、2.06%, 日内精密度5.9%~7.3%(n=6), 日间精密度5.4%~9.7%(n=6)。
为进一步考查前处理方法对目标物硝甲西泮的提取程度, 按1.3中方法处理后的样本检测结果见表3。
| 表3 标准溶液浸泡毛发样本定量检测结果 Table 3 Quantitative results of hair samples soaked in standard solution |
毛发外污染会造成假阳性结果, 因此在毛发检测中分析区分外污染和主动摄取药物是阳性结果评价必须考虑的问题, 一般有三种质控措施:临界值的确立; 优化清洗方法并收集洗液进样; 同时检测出原药和代谢物且两者成一定比例[7]。
硝甲西泮为七元环1位氮上有甲基的药物, 在体内N-甲基转移酶作用下会形成去甲硝甲西泮(母离子282)[9], 同时因其7位上含硝基, 在体内也能转化为7-氨基硝甲西泮(母离子266)[10], 已知阳性样本的一级全扫描图谱中能检出这两个离子峰, 可对其进行质谱参数的优化, 但因未购买到该两种物质可溯源标准品, 不能确证保留时间和定性离子比, 因此本实验室在阳性结果判定中采用清洗液进样进行监控, 并参考《涉毒人员毛发样本检测规范》(公禁毒〔2018〕938号)确认阈值, 在盲样检测中设置添加样的阈值进行参比。
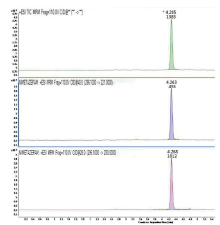
近期本州某县禁毒大队在查缉中缴获一批灰绿色片状可疑毒品, 同时当场查扣几名可疑吸毒人员, 尿检未发现阳性, 毛发快检设备初筛结果吗啡和苯丙胺都为阴性, 遂将同样毛发样本(枕部近发根端3 cm头发)两份送我实验室检验, 经过该方法的检测, 均有较好的硝甲西泮原体的响应, 如图1所示, 空白对照无干扰, 通过标准曲线计算含量分别为0.79、1.41 ng/mg, 说明近段时间摄入过该药物, 最后嫌疑人供述了服用硝甲西泮的事实。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|