第一作者简介:侯方,男,江苏徐州人,学士,助理工程师,研究方向为法医毒物。E-mail: 247299903@qq.com
目的 建立硫化氢中毒案件中硫离子的快速、准确的检验方法。方法 取血样0.4mL置于10mL玻璃试管中,加入内标1,3,5三溴苯(TBB)及衍生化试剂五氟苄基溴,放入微波合成仪60℃反应10min,离心后取有机相1μL进样GC-MS。结果 血液中硫离子在0.05~10mmol/L(1.6~320μg/mL)浓度范围内线性关系良好,检出限为0.01μg/mL,并在一起硫化氢中毒案件中成功应用。结论 本文建立的方法快捷、科学、有效,可应用于硫化氢中毒案件中的快速检测。
Objective To establish a fast and accurate method for determination of the sulfide ion in blood from cases of hydrogen sulfide poisoning.Methods Blood sample was collected of 0.4 mL and transferred into a 10-mL glass tube, together with the internal standard, 1, 3, 5-tribromobenzene, and a derived reagent α-bromo-2, 3, 4, 5, 6-pentafluorobenzyl. The sample was placed under the microwave synthesizer for 10 minutes at 60°C. After centrifugation, the organic phase (~1μL) was taken and undergone through GC-MS analysis.Results The concentration of sulfide ion in blood had good linearity in the range of 0.05-10 mmol/L (1.6-320μg/mL), with a limit of detection (LOD) of 0.01μg/mL. From the blood samples of the victims in one suspected sulfide-poisoning accident, the sulfide ion was detected successfully.Conclusions The method established here is fast, scientific and effective, therefore capable of being applied into rapid detection of hydrogen-sulfide-poisoning cases.
硫化氢(H2S)是无色气体, 具典型臭鸡蛋味。 硫化氢毒性很大, 空气中含量达到0.1%时即能引发头痛、眩晕等中毒症状, 含量达百分之几时可致人立即昏倒, 迅速死亡[1]。 硫化氢一般能在某些化学反应和蛋白质自然分解或腐败过程中产生, 接触硫化氢较多的行业有污水处理、造纸、含硫汽油的开采以及某些化学原料的制造, 沼泽地、沟渠、水井、下水道也多有硫化氢产生[2]。现有的硫化氢检验方法基本有化学法、气相色谱法、液相色谱法、离子色谱法等[2, 3, 4, 5]。化学法检验由于准确性和检测限较差, 应用较少。随着大型分析仪器的普及, 目前日本 Kage 等[6]研发的五氟苄基溴衍生化方法被广泛应用与改进, 其中代表有2012年罗才会等[7]报道的及2017年强火生等[8]报道的硫化物检验方法。其原理均为硫化氢中毒血液中多态的硫化物在碱性条件下与五氟苄基溴反应生成双五氟苄硫醚, 该产物可被有机试剂提取并可用气相色谱/质谱联用法(GC-MS)检验, 反应机理见图1。川崎医疗福利大学的Toshihiko等[9]运用了离子色谱技术检验生物检材中的硫离子等成分, 电导检测器需将硫化物用过氧化氢在碱性条件下转化为硫酸根等目标离子, 过程相对繁琐, 有条件的实验室可使用专用柱和安培检测器。本文在GC-MS法基础上引入了微波合成仪, 优化衍生化效率, 大大缩短了衍生化时间, 同时保证了检验的灵敏度, 建立起了新的微波合成/GC-MS法, 并在几起疑似硫化氢中毒案件中成功应用。
目前基层公安理化检验中, 气相色谱/质谱联用仪发挥着主力军的作用, 受仪器条件及方法限制, 在检验硫离子、氟乙酸根、吗啡等目标物时, 必须用到衍生化技术将其转化成为仪器能够检测的物质。衍生化过程一般采用恒温加热、微波衍生等手段, 其中恒温加热法所需时间较长, 通常在数小时。微波衍生法所需时间短, 但如果采用普通微波炉衍生, 重现性不能得到充分保证。本文采用具有温度、压力双重控制的微波合成仪, 实现衍生化反应条件精密控制, 从而达到高衍生效率和满足实验重现性要求。
Agilent7890B/5977AGC-MS, 配有电子轰击离子源(EI源)、Agilent Chemstation工作站; NOVA-2S型微波合成仪(上海屹尧科技)。
硫化钠、五氟苄基溴、1, 3, 5-三溴苯(TBB)、苯扎氯铵、四硼酸钠、磷酸二氢钾、乙酸乙酯、甲苯。以上试剂均为分析纯, 实验室用水为去离子水(GB/T6682规定的一级水)。
五氟苄基溴溶液:精确称取0.522 g五氟苄基溴置于100 mL容量瓶中, 后用甲苯定容。
TBB溶液:精确称取3.1 mg 1, 3, 5-三溴苯置于1 000 mL容量瓶中, 后用乙酸乙酯定容。
苯扎氯铵溶液:精确称取1.525 g四硼酸钠、0.17 g苯扎氯铵置于100 mL容量瓶中, 后用去离子水定容。
1.3.1 色谱条件
Agilent HP-5MS(30 m× 0.25 mm× 0.25 mm)毛细管柱; 柱温程序为初始温度 50 ℃, 保持 1 min后, 以 10 ℃/min 升至 280 ℃, 保持 1 min; 载气为高纯氦气, 流速 1.0 mL/min; 进样口温度 200 ℃; 传输线温度240 ℃; 进样量1 μ L; 分流比 10∶ 1。
1.3.2 质谱条件
电子轰击离子源(EI), 电子能量70 eV; 离子源温度 230℃, 四级杆温度150℃, 接口温度280℃。硫离子衍生化后生成双五氟苄硫醚C6F5CH2SCH2C6F5, 特征碎片离子质荷比为m/z 45、181、394; 内标 TBB 特征碎片离子为 m/z 233、312、154。定量时采用选择离子监测(SIM)模式, 硫离子衍生化产物和内标的定量碎片离子分别为m/z 181、312。
1.3.3 微波合成仪条件
工作模式为密闭模式, 搅拌模式打开, 化合物选为极性, 最大功率为50%; 反应温度60 ℃, 衍生化时间10 min。
取血液0.4 mL置于10 mL玻璃试管中, 加入1.5 mL苯扎氯铵(浓度为5.0 mmol/L)与四硼酸钠(浓度为0.04 mol/L)混合溶液, 然后加入20.0 mmol/L五氟苄基溴甲苯溶液1.0 mL、0.01 mmol/L 1, 3, 5-三溴苯(TBB)乙酸乙酯溶液1.0 mL, 加入磁转子后压盖密封, 漩涡震荡1 min后放入微波合成仪反应, 反应后加入0.1 g磷酸二氢钾, 漩涡振荡1 min后7000 r/min离心10 min, 分离有机相, 取有机相1 μ L进样GC-MS。
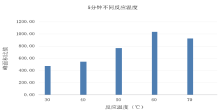
取空白血样, 添加硫化钠标准溶液使其浓度均为1.0 mmol/L。在反应时间5 min的条件下分别在30、40、50、60、70 ℃进行衍生化反应, 每个温度点取添加血样两份分别按照1.4步骤操作。质谱选用离子监测(selected ion monitor, SIM)模式, 以硫离子衍生化产物和内标物的GC-MS分析特征碎片离子m/z 181 和m/z 312的峰面积比值作为参考依据, 同一温度点的两个样取平均值。在温度条件确定后, 在该温度下分别反应3、5、10、15、20 min, 操作同上。
将试验数据整理, 绘制相应图表进行比较。从图1可以看出, 反应温度为60 ℃时, 反应效率达到最大; 从图2可以看出, 反应时间在5~15 min内比值并无明显差距, 10 min时比值较大, 因此微波合成条件选择60 ℃下反应10 min。
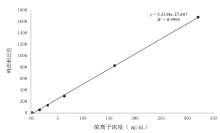
在空白血液中分别添加硫化钠溶液, 制得物质的量浓度分别为0.05、0.5、1.0、2.0、5.0、10.0 mmol/L(硫离子质量浓度分别为1.6、16、32、64、160、320 μ g/mL) 的系列样品, 分别按照 1.4 项处理后进行 GC-MS 分析, 每个质量浓度点分别进样 2个样品。以目标物和内标峰面积之比为纵坐标(y), 以硫离子的浓度(μ g/mL)为横坐标(x), 进行线性回归运算。以信噪比(S/N)≥ 3 的质量浓度为最低检出限, S/N≥ 10 的质量浓度为最低定量限。取硫离子溶液质量浓度分别为16、160、320 μ g/mL的6个平行质控样品, 按照 1.4 项处理后进行仪器分析, 在同一天内早、中、晚进行检测, 计算每个浓度样品的相对标准偏差作为日内精密度。连续测三天, 计算每个浓度样品的相对标准偏差作为日间精密度。如图3所示, 硫离子在1.6~320 μ g/mL的浓度范围内线性关系良好, 线性方程为y =5.3334x - 27.687, 相关系数为0.999 5。其最低检测限为0.01 μ g/mL, 最低定量限为0.03 μ g/mL。精密度如表1所示, 满足定量要求。
| 表1 精密度试验结果 Table 1 Results of precision assay |
2017年6月26日下午, 江苏省徐州市某路段有四名工人掉到污水监测井里, 四名工人被救出时, 一人意识模糊, 仍有生命体征, 另外三人意识较清晰, 四人被送往医院救治, 同时抽血送检, 在血液中检出硫离子, 迅速向事发地公安机关反馈, 经医院抢救, 1名工人死亡, 3名工人脱离危险, 采用标准曲线法进行定量检验, 该名死亡工人血液中硫离子的质量浓度为45.8 μ g/mL。
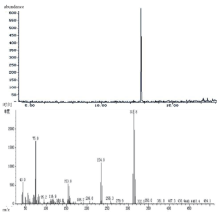
本实验室条件下, 硫离子衍生化产物的保留时间为15.249 min, 特征离子为m/z 181、394、45, 内标的保留时间为12.766 min, 相关图谱见图4~5。
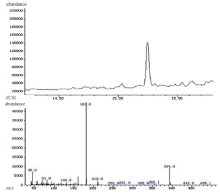 | 图4 硫离子衍生化产物色谱(上)与质谱(下)图Fig.4 Chromatogram (top) and mass spectrogram (bottom) of the sulfide-ion derivative |
硫化氢中毒案件一般具有中毒人数多、社会影响大、舆论关注强烈的特点, 这也就导致了公安检验人员在检验此类案件时在时间上有着巨大的压力, 如何在保证科学、准确的前提下更快捷地检验血液中的硫离子一直是公安实战中急需攻克的难题。本方法通过引入微波合成仪作为反应平台, 优化衍生化条件, 成功建立了硫化氢中毒案件血液中硫化物的快速检验法, 极大地缩短了检验时间。该方法有着操作简单、检验时间短、灵敏度高、稳定性好的优点, 解决了公安实战中硫离子检验的难题, 具有重要意义。在检验的同时, 应注意到由于血液中存在内源性硫离子以及检材保存、腐败产生等问题, 硫化氢中毒的结果解释与评价一直是法医毒物学的难点问题, 目前公认的空白血液中硫离子质量浓度低于0.05 μ g/mL[8] , 因此在检验时, 应结合实验室相应条件、方法特性, 通过调整反应的血液量、样品进样量、仪器分流比等各种参数, 使空白血液样品不出现硫衍生物的特征色谱峰, 再根据案情需要, 对血中硫离子进行定量检验, 综合判断后得出客观准确的结论。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|