第一作者简介:李想,女,山东蓬莱人,硕士研究生,研究方向为刑事毒物分析。E-mail:244843854@qq.com
* 通讯作者简介:朱昱,男,辽宁沈阳人,硕士,教授,研究方向为毒物毒品检验。E-mail:zhuyuzhuyu@sina.com目的 建立血中氰离子的衍生化气相色谱-质谱联用(GC/MS)分析方法。方法 血液样品依次加入苯胺的环己烷溶液、亚硝酸钠溶液以及盐酸溶液,涡旋混合。再加入硫酸铜溶液,混匀后放入50℃水浴加热15min。离子肼气质联用法(GC-MS/MS)检测衍生物苯甲腈和内标物氯代苄。采用标准品衍生物的标准质谱图定性分析,选择 m/ z 76(苯甲腈二级质谱特征峰), m/ z 65(氯代苄二级质谱特征峰)作为定量离子进行定量分析。结果 血中氰离子的最低检出限为0.05µg/mL,提取回收率为95%。结论 该方法专属性强,操作简便,适用于血中氰离子检测。
Objective To establish a GC/MS/MS derivatization method for determining the cyanide in blood.Methods Blood sample was sequentially added with the solutions of aniline cyclohexane, sodium nitrite and hydrochloric acid, then being subjected to vortex for mixing. After one more addition of copper sulfate solution into the above sampling blood, the mixture was heated at 50℃ for 15 min, thus resulting in the benzyl cyanide/chloride to be determined by GC/MS/MS, with the ions m/z 76 and m/z 65 for quantitative analysis of characteristic peak from benzyl cyanide/chloride.Results The cyanide ions in blood sample showed the limit of detection as 0.05 µg/mL and the average recovery about 95%.Conclusion This method is of specificity, rapid for qualitative analysis of cyanide in blood.
氰化物是毒性强, 作用快的毒物之一。目前对生物检材中氰化物的检测方法报道不多, 主要用离子色谱法[1]、衍生化分光光度法[2] 、顶空气质联用法(GC/MS)[3]、衍生化色阶法[4]、衍生化顶空气相色谱法[5]、衍生化顶空气质联用法(GC/MS)[6]、衍生化三重四极杆气质联用法(GC-MS/MS)[7, 8]。这些方法各有不足之处:离子色谱、衍生化分光光度检测方法, 受样品基质中共存离子的干扰和仪器设备的限制较大; 顶空GC/MS检测方法需将氰离子转化为HCN, HCN挥发性强, 且其分子量过小, 其质谱特征性差; 衍生化色阶法、衍生化顶空气相色谱法、衍生化顶空GC/MS检测方法, CN-衍生化氯化氰或溴化氰进行分析, 定性分析时特异性均较差, 易受血、尿等检材中易挥发的内源杂质干扰; 文献[7]所用衍生化GC-MS/MS方法采用分子量较大的衍生化试剂, 因而所生成衍生物的离子质核比较大, 具有较高的特征性。但检测仪器用气质相色谱没有电子捕获检测器进行检测的灵敏度高。文献[8]所用衍生化GC-MS/MS方法采用萘基作为衍生化试剂, 所生成衍生物的离子m/z较大, 具有较高的特征性, 但萘胺在环己烷中的溶解度不好, 衍生化过程重现性不佳。本文选用苯胺作为衍生化试剂与亚硝酸盐生成重氮盐, 重氮盐在亚铜离子的催化下与氰根发生桑德迈尔反应, 生成氰基苯, 用GC/M-S/MS检测衍生化产物。
仪器:Thermo-Finnigan PolarisQ离子阱质谱联用仪(配置MS/MS); HC-3018型离心机(安徽中科中佳科学仪器有限公司); 涡旋器(江苏金坛机械厂)。
试剂:苯胺(99.5%, 沈阳市试剂一厂); 氯代苄、亚硝酸钠、硫酸铜、盐酸(均为分析纯, 国药集团化学试剂有限公司); 氰离子标准溶液(100 µ g/mL, 北京坛墨质检科技有限公司); 空白血为健康人血; 水为去离子水。
色谱条件:色谱柱:DB-5MS(30 m× 0.25 mm i.d. × 0.25 μ m)。程序升温:60 ℃开始, 保持1 min, 以20 ℃/min升至80 ℃, 保持0 min, 以5 ℃/min升至95 ℃, 保持0 min, 以20 ℃/min升至280 ℃。进样口温度:280 ℃。
质谱条件:电子轰击源能量70 eV; 离子源温度200 ℃; 传输线温度280 ℃; 溶剂延迟时间3 min; 一级质谱扫描模式(50~200, m/z); 二级质谱SRM检测母离子m/z 76(苯甲腈), m/z 65(氯代苄)。
标准添加血样溶液:临用时在血液中添加氰离子标准溶液, 形成0.1、0.5、1、2、4、8、10 µ g/mL系列浓度的标准浓度血样。
氯代苄内标溶液配制:准确移取23 µ L氯代苄液体用甲醇定容至25 mL, 浓度为1.0 mg/mL。
苯胺衍生化试剂配制:准确移取25 µ L苯胺液体用环己烷定容至25 mL, 浓度为0.15 mol/mL。
NaNO2溶液配制:准确称取1.25 g NaNO2固体用去离子水定容至25 mL, 浓度为50 mg/mL。
CuSO4溶液配制:准确称取0.4 g 无水硫酸铜固体用去离子水定容至25 mL, 浓度为0.1 mol/L。
HCl溶液配制:准确移取52 µ L浓盐酸液体用去离子水定容至25 mL, 浓度为1.0 mol/L。
取血样1 mL, 加5 µ L内标溶液, 涡旋离心。依次加入0.25 mL苯胺衍生化试剂, 0.5 mL NaNO2溶液, 0.05 mL HCl溶液, 以及0.1 mLCuSO4溶液, 涡旋混合1 min。放入50 ℃水浴加热15 min。将混合液涡旋后离心, 取有机相1 µ L, 备检。
苯胺衍生化方法为两步衍生化方法, 先由苯胺与亚硝酸盐生成重氮盐, 苯胺与亚硝酸盐的配比直接影响衍生化结果。本文分别考察了苯胺与亚硝酸盐的用量, 当苯胺用量多于亚硝酸盐用量时, 实验效果最佳, 但苯胺用量过大, 衍生化试剂很难除去, 衍生化反应之后剩余的衍生化试剂除去困难或剩余量过大, 进入有机相中的衍生化试剂量也就越多, 色谱本底信号就越强, 对检测造成干扰的可能性就越大。本文对浓度为0.15 mol/mL的苯胺试剂在用量分别为0.05、0.1、0.2、0.25、0.5 mL条件下进行了考查(图1a), 实验结果表明, 当CuSO4溶液的用量为0.1 mL, 50 ℃水浴加热15 min后, 加入苯胺试剂0.25 mL以上时, 苯甲腈与氯代苄的定量色谱峰面积之比达到恒定值, 故本文选择苯胺的用量为0.25 mL。硫酸铜作为第二步衍生化反应的催化剂, 不但能有效催化衍生化反应, 也能提高衍生化速度。本文考察了0.02、0.06、0.08、0.1、0.2 mL硫酸铜用量对衍生化反应的影响(图1b), 研究发现, 使用0.1 mL浓度为0.1 mol/L的CuSO4溶液, 能达到最佳衍生化效果。由于苯胺衍生化反应需要在酸性条件下进行, 本文考察了酸度对衍生化反应的影响。由于盐酸在第二步衍生化时, 会与氰离子产生竞争, 当盐酸用量过大时, 氰离子很难与重氮盐结合。而盐酸用量过小又会使第一步衍生化很难进行。所以本文对0.01、0.02、0.04、0.05、1 mL盐酸对衍生化反应的影响进行了考察(图1c), 发现当使用浓度为1 mol/L盐酸溶液0.05 mL时, 衍生化效果最好。
 | 图1 衍生化效率的影响(a:试剂; b:催化剂用量; c:酸性试剂用量)Fig.1 The influence on the derivatization(a. reagent; b. catalyst quantity; c.acidic reagent quantity) |
本文在选择内标时, 选用氯代苄作为内标, 同时也考察了与苯甲腈结构相近的甲苯、氯苯、溴代苄。但甲苯与提取溶剂环己烷保留时间重叠, 质谱相互干扰; 氯苯是苯基衍生化反应副产物; 溴代苄的保留时间与衍生化中间产物硝基苯的保留时间相同。只有氯代苄与分析物结构性质、色谱行为等相近, 且色谱峰完全分离, 质谱无干扰。所以本文选择氯代苄作为衍生化内标物。
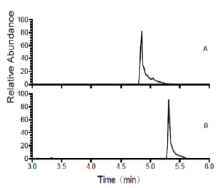
本文所选程序升温在目标峰出峰时间段降低升温速率, 以保证更好地分离目标峰。苯甲腈和氯代苄总离子流色谱和二级质谱表明, 各色谱峰分离良好, 相互之间无干扰, 苯甲腈保留时间4.9 min、氯代苄保留时间5.3 min。
本文选择的母离子为一级质谱的特征离子, 因为一级质谱中特征离子的丰度高, 特征强, 干扰小。苯甲腈和氯代苄的一级质谱特征离子为m/z 103和m/z 91。本文对各衍生物在1.00、1.50和2.00 V激发电压下, 进行二级质谱检测, 结果表明, 当激发电压为1.50 V时, 离子基本解离。在优化好的条件下, 分别得到苯甲腈和氯代苄的二级质谱图(图2), 其二级质谱特征离子分别为m/z 76和m/z 65。
标准添加血样按1.4项方法操作, 分别记录数据, 以苯胺浓度为横坐标, 以苯胺与氯代苄峰面积比值为纵坐标, 以最小二乘法回归计算, 得到标准曲线回归方程为y=0.335x+0.04, r=0.9980。结果表明, 苯甲腈在此色谱条件下0.1~10 µ g /mL浓度范围内, 线性关系良好, 可以满足毒物分析工作要求。按信噪比3∶ 1确定最低检测限, 最低检测限为0.05 µ g/mL。按信噪比10︰1确定定量限, 定量限为0.18 µ g /mL。
取标准添加血样高、中、低3个浓度(分别为0.1、2、10 µ g/mL), 按1.4项操作。按实验方法平行操作6次, 结果见表1, 计算平均相对回收率为95%, 日内RSD为4.52%。
| 表1 血中衍生化GC/MS/MS分析的精密度和准确性(n=6) Table 1 Recovery and precision of naphthyl derivatives in the tested blood by GC/MS/MS (n=6) |
本文建立了血中氰离子的苯胺衍生化GC-MS/MS分析方法, 避免了传统方法中提取率低, 氢氰酸挥发损失较大的弊病。GC-MS/MS显示出专属性强、灵敏度高等特点。在实际案例中的应用证明该检测方法满足司法鉴定工作的要求。
The authors have declared that no competing interests exist.
作者已声明无竞争性利益关系。The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|