作者简介:高中勇(1975—),男,山东汶上人,硕士,工程师,研究方向为理化检验。E-mail: gzymba@163.com
目的 血液中苯酚检测。方法 采用乙酸乙酯液液萃取,GC/MS分析。结论 血液中苯酚的回收率为95.8%,方法的工作曲线为 y=525069 x-59076, r2=0.999,线性范围为0.1~10μg/mL,检出限为0.01μg/mL(S/N=3.8)。结论 本方法操作简便,适合于血液、胃内容、脏器等生物检材中苯酚的定性定量分析,可在案件检测中使用。
Objective To determine phenol in blood.Methods The sample was extracted with ethyl acetate, and then subjected to GC/MS analysis.Results The recovery was 95.8% of the phenol in blood, with the working curve of the used method being y=525069 x - 59076, and the correlation coefficient as r2=0.997. The linear range was 0.1 to 10 μg/mL, and the detection limit being 0.01 μg/mL (S/N=3.8).Conclusion The method is simple and suitable for both qualitative and quantitative analysis of phenol in evidential materials such as blood, stomach fluid, viscera and the others, therefore capable of being used in case detection.
苯酚(phenol, C6H5OH)广泛应用于消毒剂、防腐剂、医用漱口水和润喉片等医药品的生产, 工业上作为酚醛树脂的原料。但是苯酚具有一定的毒性及黏膜腐蚀性, 长期接触可出现头痛、眩晕症状, 严重者可发生精神障碍[1], 抑制中枢神经系统, 引起肝、肾功能损害。由于苯酚有特殊气味, 其中毒多为职业性, 罕见他杀。近年来, 却常有非法行医者将其作为皮肤病的治疗药物, 因用量不当导致中毒, 甚至死亡。
苯酚检测已报道采用高效液相色谱法[2]、光度法[3]、毛细管电泳法[4]、气相色谱质谱法, 但是这些方法主要集中在环境样品、水质、食品检测等方面, 在生物样本中的检测较少。笔者采用液液萃取法对血液中苯酚进行提取、GC/MS检测, 并将该方法应用到案件检测中, 收到良好的效果。目前对于苯酚接触人群, 常通过对其血液中游离苯酚含量测定作为确定试验[5]。
苯酚对照品1 mg/mL(液态, 基体为0.02 moL/L氢氧化钠, 北京海岸鸿蒙提供)。将标准品稀释成0.1 mg/mL标准工作液(该对照品基体为强碱性物质, 仅用于向空白血液中添加, 不直接进行GC/MS分析), 4 ℃冰箱保存; 空白血购于本市血站, 为健康成人血液。
7890A-5975C型GC /MS仪, 配自动进样器(美国安捷伦公司); SK-Ⅰ 型MSD快速混匀器(江苏金坛市顺华仪器有限公司); 超声波清洗器:KQ-500DE型, 昆山市超声仪器有限公司; D10-12型氮吹仪(杭州奥盛); 5804R高速离心机(德国Eppendorf公司) 。
取血样1 mL, 加5 mL乙酸乙酯, 震摇10 min, 8000 r/min离心, 取上清液至尖底玻璃试管中, 重复上述步骤两次, 合并上清液, 室温氮吹, 浓缩至干, 100 μ L甲醇定容, GC/MS进样分析, 进样量1 μ L。如果血液中苯酚含量较高, 可在检测时将血液按一定量稀释, 再进行提取检测, 同时在进行空白添加时, 应将空白血等倍进行稀释。
1.3.1 色谱柱 DB-5MS(30 m× 0.25 mm× 0.25 μ m)弹性石英毛细柱。
1.3.2 定性测定 柱温:初始温度80 ℃, 保持1 min, 以10 ℃/min的速率升至280 ℃, 保持15 min; 进样口:280 ℃; 离子源温度:230 ℃; 传输线温度:280 ℃; He流速:1 mL/min; 进样方式:分流进样, 分流比20:1; EI源:70 eV; 扫描方式:scan; 扫描范围(m/z):40~450 amu, 溶剂延迟3 min。
1.3.3 定量测定 扫描方式为SIM, 选择离子为m/z 94。
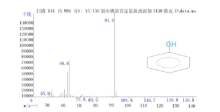
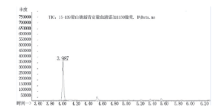
苯酚标准溶液经GC/MS分析, 将标准溶液在扫描模式下进行测定, 确定其质谱结构信息和保留时间, 选择丰度高、碎片质量较大、干扰少的离子作为定量和定性离子, 其TIC图与质谱图见图1、图2。空白血液及添加TIC图见图3和图4。标准溶液中苯酚的保留时间为4.037 min(见图1), 血液添加中苯酚的保留时间为3.987 min, 两者保留时间一致, 特征离子均为m/z 55、66、94, 可以准确定性; GC/MS分析血液中苯酚, 加标样品的色谱图峰形良好, 空白无杂质干扰, 说明此仪器方法条件的适用性良好。
在液液萃取中, 萃取溶剂的选择至关重要, 直接影响到苯酚的萃取效率。本文根据苯酚的溶解性和基质特点, 选取了乙酸乙酯、苯、氯仿、乙醚等四种有机溶剂。取空白血1 mL, 添加5 μ g苯酚, 血液在不调酸碱的情况下分别用以上四种溶剂进行提取, 按1.2、1.3方法平行双样操作, 结果得到四种提取溶剂对苯酚的回收率从高到低依次为苯(98.7%)> 乙酸乙酯(96.5%)> 乙醚(88.4%)> 氯仿(83.3%)。虽然苯的提取率略高于乙酸乙酯, 但是由于苯的毒性大, 对操作人员的健康不利, 故最终选择乙酸乙酯作为提取溶剂。进一步考察超声提取和振荡提取两种常见的提取方式对提取效率的影响, 结果表明两种提取方式对结果的影响接近, 由于振荡提取操作简单, 故选择该提取方式。
取空白血1 mL, 添加苯酚标准品使其添加浓度分别为1.0、0.5、0.1 μ g/mL, 按1.2、1.3步骤进行回收率测定, 结果依次为108.2%、82.8%、86.5%。空白加标回收率为82.8%~108.2%, 参照GB/T27404-2008[6]对方法回收率的规定, 满足要求。
取5份1 mL空白血, 分别添加苯酚0.1、0.5、1.0、5.0、10.0 μ g, 按1.2步骤提取, GC/MS检测, 做方法工作曲线。以浓度为横坐标, 以特征离子m/z 94峰面积为纵坐标绘制线性回归曲线, 回归方程为y=525069x-59076, 相关系数为0.999, 检出限为0.01 μ g/mL(S/N=3.8)。
据报道, 健康人血液中有时也会产生微量的苯酚, 谭家镒等人对健康男性青年凌晨空腹采集的血液进行苯酚含量的测定, 结果为(2.2± 0.4)μ g/mL[7], 但是健康人员中苯酚含量阈值目前还没有确切的报道, 有待进一步研究。笔者经过对多起苯酚中毒人员的血液检测, 血液中苯酚浓度在46.76 μ g/mL以上, 远远大于上述报道, 这也与文献报道苯酚致死血浓度为50~250 μ g/mL[8]相一致。在进行血中苯酚定量检测时, 应先对空白血进行检测, 筛查出不含苯酚的血液进行空白对照和添加对照试验。
血液中苯酚含量随着腐败而迅速降低, 目前还未见文献报道苯酚在不同温度、环境下降解变化规律, 对于苯酚中毒的案件应及时送检并低温保存, 防止苯酚降解, 影响血液中苯酚含量的检测结果。谭家镒等人采用GDX403固相萃取小柱萃取血液中的苯酚、甲酚等, 回收率为97.8%~104%, 效果良好, 但是GDX403固相萃取柱不仅在市面上很少见, 而且价格高、检材量消耗大。本文方法检材消耗量少, 最少可用0.1 mL即可满足检验要求, 操作简便, 成本低, 非常适合基层一线检测需要。
姚某青(女, 56岁)因患头皮癣, 购买了不明成分的药水进行治疗。2015年3月31日, 在家中用该药水洗头时倒地身亡。提取心血、胃组织、肾脏、肝脏、头部皮肤组织等生物检材及盛药水的药瓶(瓶内剩余黄褐色液体约2 mL, 有强烈的特殊气味), 按照本文方法进行检测, 其中心血检测所得总离子流图见图5。样品保留时间为4.123 min, 与苯酚标准品及空白血添加中苯酚相比较, 色谱峰保留时间和特征离子碎片均一致。按照本方法, 对胃组织等其余检材进行了检测, 均检出苯酚成分, 其中心血中含量为46.76 μ g/mL, 胃组织含量为6.41 μ g/mL。
本文所建方法中苯酚色谱峰峰形好, 检测灵敏度高, 重现性好, 线性范围广, 适合于血液、胃内容物等生物检材中苯酚的定性定量分析, 亦可以分析可疑药物中苯酚成分及含量, 经实际案件检验验证, 适于中毒案件中苯酚的定量检验。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|