作者简介:张大雷(1977—),男,黑龙江大庆人,高级工程师,博士,研究方向为理化检验技术。E-mail:zdlahf@163.com
目的 建立人体全血中4-溴-2, 5-二甲氧基苯乙胺的衍生化GC/MS分析方法。方法 血液样品经去离子水稀释4倍,8000r/min高速离心20min后,加入NaH2PO4缓冲溶液(pH值为6.0)2mL,混匀。将上述混合液加入用甲醇、NaH2PO4缓冲溶液(pH值为6.0)活化的Bond Elut Centify®固相萃取柱后,依次采用1.0M乙酸溶液、去离子水、甲醇、二氯甲烷/异丙醇/氨水(78/20/2,V/V/V)混合洗脱液进行提取、分离、净化处理,40℃空气流下挥干,三氟乙酸酐衍生化,GC/MS检测4-溴-2, 5-二甲氧基苯乙胺和4-苯基丁胺衍生物。采用标准品衍生化产物的标准质谱图定性分析,选择m/z 242(4-溴-2, 5-二甲氧基苯乙胺)、m/z 91(4-苯基丁胺)作为定量离子进行定量分析。结果 血液中4-溴-2, 5-二甲氧基苯乙胺的最低检出限为6ng/mL,在0.02~10µg/mL浓度范围内,线性关系良好(=0.9993),日内精密度和日间精密度均小于10%,平均提取回收率约为69%。结论 该方法操作简便、灵敏度高,适用于全血中4-溴-2, 5-二甲氧基苯乙胺检测。
Objective To establish a GC/MS derivatization method for determining the 4-bromo-2, 5-dimethoxy-phenethylamine in blood.Methods Blood sample was extracted and purified by Bond Elut Centify® solid phase extraction column after diluted to four times by deionized water. The residuum was derivatized by trifluoroacetic anhydride. 4-bromo-2, 5-dimethoxyphenethylamine and 4-phenylbutylamine (internal standard) were analyzed by gas chromatography-mass spectrum. The ions m/z 242 and m/z 91 were applied in quantitative analysis for 4-bromo-2, 5-dimethoxyphenethylamine and 4-phenylbutylamine, respectively.Results The limit of detection was 6 ng/mL in blood sample and the calibration curve was linear in the range of 0.02~10μg/mL (=0.9993) for 4-bromo-2, 5-dimethoxyphenethylamine. The RSDs of intra-day and inter-day were less than 10%; the average extraction recovery of 4-bromo-2, 5-dimethoxyphenethylamine was about 69%.Conclusions This method is rapid, sensitive and suitable for qualitative analysis of 4-bromo-2, 5-dimethoxyphenethylamine in blood.
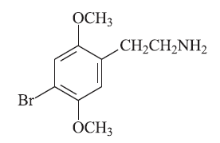
4-溴-2, 5-二甲氧基苯乙胺(2C-B)1974年由Alexander Shulgin首次合成并发现其有精神作用[1]。上世纪90年代开始, 一些国家先后发现该物质出现被滥用的情况, 随即WHO和美国、瑞士等国家相继将其列为管制药品并禁止使用[2, 3, 4]; 我国于2001年将其列入Ⅰ 类精神药品品种目录[5]。有报道称该化合物具有兴奋和致幻双重精神作用, 强度是4-溴-2, 5-二甲氧基苯丙胺强的10倍。随着服用剂量的升高, 首先出现兴奋、松弛、消极的精神感觉, 并随着剂量的增加不断增强, 同时各种感官出现不同程度的欣快、兴奋, 最后直至出现幻觉或达到妄想的状态, 持续时间可达到6h左右, 会引起身体严重的毒性副作用[1, 3, 6]。4-溴-2, 5-二甲氧基苯乙胺的化学结构见图1。
目前国际上对生物检材中的4-溴-2, 5-二甲氧基苯乙胺的检测方法报道不多, 主要是采用液-液或固相萃取的方法提取生物检材后, 采用气相色谱法(GC)、气相色谱-质谱联用法(GC/MS)、高效液相色谱法(HPLC)和液相色谱-质谱联用法(LC/MS)分析4-溴-2, 5-二甲氧基苯乙胺原体成分[6, 7, 8, 9]。国内尚无血液中检测方法报道。鉴于生物检材的基质干扰及该化合物的信号响应低等情况, 为提高检验的灵敏度, 本文拟建立衍生化GC/MS法检测血液中4-溴-2, 5-二甲氧基苯乙胺的方法, 为今后法医毒物分析和吸毒人员检测提供灵敏、快速的分析方法。
仪器:7890A/5975C气质联用仪, 配EI源(美国Agilent公司); TJ-6高速离心机(美国BECKMAN公司); VORTEX-GENIE 2旋涡混合器(美国Scientific Industries公司); Milli-Q超纯水机(美国Millipore公司); AB135-S分析天平(瑞士METTLER TOLEDO公司, 0.01mg); pH计(瑞士METTLER TOLEDO公司); DSY-Ⅱ 型自动快速浓缩仪(北京金科精华苑技术研究所); CNW 12固相萃取装置(德国CNW公司); Bond Elut Centify® SPE柱(填料:C8和苯磺酸, 3mL, 美国Agilent公司)。
试剂:4-溴-2, 5-二甲氧基苯乙胺盐酸盐(纯度95%, 黑龙江大学化学化工学院合成); 4-苯基丁胺(SIGMA-ALDRICH公司, 纯度 98%, 密度 0.944); 甲醇、二氯甲烷、异丙醇、乙酸乙酯(DIKMA公司); 氨水、三氟乙酸酐、NaH2PO4(SIGMA-ALDRICH公司)。
色谱条件:色谱柱:Agilent DB-1MS(30m× 0.25mm× 0.25μ m); 程序升温:110℃开始, 保持2min, 以10℃/min升至280℃, 保持15min; 进样口温度:250℃; 载气:高纯He, 流速1mL/min; 进样量:1μ L。
质谱条件: MSD传输线温度270℃; 离子源温度230℃; 四极杆温度150℃; 电子轰击源能量:70eV; 溶剂延迟时间:3.5min; 全扫描模式(40~500, m/z); 选择离子扫描 m/z 242(4-溴-2, 5-二甲氧基苯乙胺), m/z 91(4-苯基丁胺)。
标准溶液:精密称取4-溴-2, 5-二甲氧基苯乙胺盐酸盐0.01201g于10mL容量瓶中, 甲醇定容, 配成浓度为1mg/mL的标准储备液; 临用时用甲醇稀释成0.5, 25, 50, 100, 150, 200, 250μ g/mL的系列浓度的标准工作液。
内标溶液:精密称取4-苯基丁胺2.700mL于25mL容量瓶中, 甲醇定容, 配成浓度为0.1 mg/mL的内标工作液。
提取:取血液样品0.5mL, 加入2μ g 4-苯基丁胺(内标), 去离子水稀释4倍, 8000r/min离心20min, 取上清液, 加入NaH2PO4缓冲溶液(pH值为6.0)2mL, 混匀。
净化:依次用2mL甲醇, 2mLNaH2PO4缓冲溶液(pH值为6.0)活化固相萃取柱。将处理过的血液样品加载过柱后, 依次用1.0 mol/L乙酸溶液1mL, 去离子水3mL淋洗, 甩干小柱; 再用甲醇6mL淋洗, 8000r/min离心5min, 甩干小柱; 3mL二氯甲烷/异丙醇/氨水(78/20/2, V/V/V)混合溶液洗脱, 40℃空气流下挥干。
衍生:向挥干洗脱液的试管中加入乙酸乙酯、三氟乙酸酐(TFAA)各30μ L, 密封, 60℃水浴30min, 取出挥干, 50μ L乙酸乙酯定容。
空白血液中添加一定浓度4-溴-2, 5-二甲氧基苯乙胺工作液和内标, 按1.4项操作, 研究了不同初始温度和升温速率对检测结果的影响, 得到1.2项条件符合4-溴-2, 5-二甲氧基苯乙胺检测的需要, 见图2。同空白血液同法操作后比较, 结果为4-溴-2, 5-二甲氧基苯乙胺衍生产物和内标4-苯基丁胺衍生产物的保留时间分别为13.3min和8.7min, 理论塔板数按4-溴-2, 5-二甲氧基苯乙胺衍生产物计算不低于1.0× 104, 血液中内源性物质不干扰4-溴-2, 5-二甲氧基苯乙胺和内标的检测。
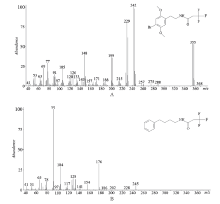
在优化好的条件下, 分析后得到4-溴-2, 5-二甲氧基苯乙胺衍生产物和内标4-苯基丁胺衍生产物的特征质谱图, 如图3。采用选择离子监控模式(SIM)进行定量分析, 其定量离子分别为m/z 242和m/z 91。
精密量取空白血液0.5mL, 分别加入不同浓度的4-溴-2, 5-二甲氧基苯乙胺系列标准溶液20μ L、内标工作液20μ L, 制成血浆中4-溴-2, 5-二甲氧基苯乙胺浓度分别为0.02、1、2、4、6、8、10 μ g/mL的血液添加样品。按1.4项下方法操作处理, 分别记录分析所得数据。以4-溴-2, 5-二甲氧基苯乙胺浓度为横坐标, 4-溴-2, 5-二甲氧基苯乙胺与内标物峰面积比值为纵坐标, 以最小二乘法回归运算, 得到标准曲线回归方程为Y = 0.299X + 0.05, r = 0.9993。结果表明, 4-溴-2, 5-二甲氧基苯乙胺在此色谱条件下0.02~10μ g/mL浓度范围内, 线性关系良好, 可以满足临床药物监测和法医毒物分析实际工作需要。
按信噪比为1: 3确定最低检测限、信噪比为1: 10确定定量限。测得4-溴-2, 5-二甲氧基苯乙胺最低检测限为6ng/mL, 定量限为17ng/mL。
取空白血液0.5mL, 按照2.3方法配制4-溴-2, 5-二甲氧基苯乙胺高、中、低3个浓度(分别为10、4、0.02μ g/mL)的质控样品, 按1.4项操作处理, 测定3d, 得4-溴-2, 5-二甲氧基苯乙胺与内标物峰面积比值, 按照线性回归方程计算准确度、日内和日间精密度。结果见表1, 高、中、低浓度(10、4、0.02μ g/mL)血样测定准确度分别为101%, 95%和97%, 日内和日间RSD均小于10%。
| 表1 血液中4-溴-2, 5-二甲氧基苯乙胺的精密度、提取回收率(n=5) Table 1 Precision and recovery of 4-bromo-2, 5-dimethoxyphenethylamine in human blood (n=5) |
取空白血液0.5mL, 按照2.3方法配制4-溴-2, 5-二甲氧基苯乙胺高、中、低3个浓度(分别为10、4、0.02μ g/mL)的血液样品各5份, 按1.4项操作处理, 得4-溴-2, 5-二甲氧基苯乙胺衍生物峰面积A1。取空白血液 0.5mL, 直按1.4项操作处理后, 添加相应4-溴-2, 5-二甲氧基苯乙胺标准工作液各5份, 衍生化、吹干、溶解后进样, 得4-溴-2, 5-二甲氧基苯乙胺衍生物峰面积A2。
回收率公式为:回收率= A1 / A2× 100%。按照公式计算, 测得的回收率见表1, 平均回收率为69.5%。
本方法选用应用广泛的GC/MS作为分析仪器, 适应当前药物检测和法医毒物分析工作的需要, 经过反复进样分析, 确定起始温度为110℃, 升温速率不宜过快, 为10℃/min, 较好地保证了被检测组分的完全分离。结果表明, GC/MS 对该化合物的响应值好, 检测灵敏度高, 适用于血液样品中4-溴-2, 5-二甲氧基苯乙胺成分的分析。
4-溴-2, 5-二甲氧基苯乙胺属于苯乙胺类化合物, 由于结构中含有氨基, 化合物呈碱性, 选用阳离子交换SPE柱进行样品的提取、净化处理, 可消除血液中酸性、中性化合物对检测的干扰。Theobald DS等曾报道过体内生物样品中碱性药品使用碱性阳离子交换SPE柱进行样品的前处理方法, 这与本方法选用varian Bond Elut Centify® SPE柱处理样品的原理相同[10, 11, 12]。本研究选用该SPE柱处理4-溴-2, 5-二甲氧基苯乙胺可以达到较好的样品前处理效果, 血液添加样品的提取回收率高, 效果较好。
三氟乙酸酐作为常用的衍生化试剂运用于本方法中, 不仅可以提高产物的气化效果, 而且可以增加质谱的响应值, 进而提高了检测灵敏度。有报道称应用三氟乙酸酐衍生化的方法检测生物样品中甲基苯丙胺、氯胺酮等毒品成分, 使检测的灵敏度有较大提高[13, 14]。研究选用三氟乙酸酐作为衍生化试剂, 衍生化产物产率高、稳定性好, 其他干扰物质衍生化产物不影响4-溴-2, 5-二甲氧基苯乙胺定性、定量分析。
目前, 4-溴-2, 5-二甲氧基苯乙胺作为新兴毒品成分, 已在我国发现并有逐步扩大滥用的趋势。建立血液样品中该成分的分析方法势在必行, 本研究建立了固相萃取方法提取、净化血液中4-溴-2, 5-二甲氧基苯乙胺成分, 采用衍生化GC/MS全扫描方法进行定性分析, 选择离子模式进行定量分析。方法简便、灵敏、可靠, 适用于吸毒人员临床药物监测和法医毒物分析的需要。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|