作者简介:杨 帆(1987—),男,山东人,硕士研究生,主要从事法医遗传方面的研究工作。Tel:15618132472; E-mail:afantiyf007@gmail.com
目的 建立荧光原位杂交(FISH)联用激光捕获显微分离技术(LCM)精确分离男女混合斑中精子的检验方法。方法 收集健康志愿者精子和女性阴道上皮细胞制备模拟混合斑,经过预处理后用Vysis CEP®X SpectrumOrangeTMY SpectrumGreenTM试剂盒进行荧光原位杂交,并用PALM激光捕获显微分离系统分离男、女性细胞,使用Identifiler试剂盒结合低体积扩增技术分别对男女成分进行STR扩增。结果 荧光原位杂交后,可清晰分辨混合斑中的男女细胞。捕获20个精子细胞可以得到完整的STR分型,检出率为80%。随着精子数目增多,检出率提高而等位基因丢失率降低。30个精子检出率最高,为95%。结论 激光捕获显微分离联用FISH技术可用于混合斑中男女细胞DNA的分离检验。
Objective To establish a method for isolating spermatozoa from epithelial cells in male-female mixtures by fluorescence in situ hybridization and laser capture microdissection. Methods Male sperm and female vaginal epithelial cells from two volunteers were collected and mixed with each other, CEP®X SpectrumOrangeTM Y SpectrumGreenTMkits was used to hybridize the mixtures, and then the male and female cells were collected selectively by laser capture microdissection. Finally, a multiplex PCR was performed by the Identifiler kit using the on-chip LV-PCR. The cells found to contain only a single orange(X)or a single green(Y) were classed as spermatozoa, where as cells found to contain both an orange and a green were considered as epithelial cells. Results The completed STR typing was obtained from 20 sperm cells. The more cells were analyzed, the higher recovery rates and lower allelic dropout rates were got. With 30 sperm cells, the highest recovery rate (95%) was obtained. Conclusions The combination of Fluorescence in situ hybridization and laser capture microdissection is effective for genotyping sperm from sperm/epithelial cell mixtures.
中图分类号:DF793.2 文献标识码:A 文章编号: 1008-3650(2014)06-0014-03
混合斑是常见的混合生物检材, 也是法医DNA检验的疑难检材之一。需要将精子细胞分离并单独扩增以获得其遗传分型。当女性物质较多而精子细胞相对较少时, 传统的差异裂解法往往不能将女性成分完全分离, 单细胞分离技术为混合斑检验提供了新途径[1, 2, 3, 4]。对于较新鲜的检材来说, 精子细胞形态完整, 显微镜能够清晰观察, 单细胞分离技术取得了很好的效果。然而, 某些保存条件差或时间较长的检材, 精子形态往往不典型, 仅仅凭借形态学的观察很难同细胞碎片或杂质区分开来, 如果检材中的精子量少, 则更难捕获到真正的精子。荧光标记的方法可以便于混合斑中精细胞的识别[5, 6, 7]。前期相关专家基于荧光原位杂交和激光捕获显微分离技术, 建立了男女混合血分离检验技术[8, 9]。本文建立了适合精子细胞荧光标记方法, 并将其用于混合斑中精细胞的分离检验。
Vysis CEP® X SpectrumOrangeTMY Spectrum-GreenTM 试剂盒(Vysis公司, 美国); Vysis FISH Pretreatment Reagent 试剂盒(Vysis公司, 美国); AmpFlSTR® IdentifilerTMPCR Amplification Kit试剂盒(AB公司, 美国); ThermoBriteTM分子杂交仪(Thermo公司, 美国); PALM激光捕获显微分离系统(ZEISS公司, 德国); ASN400E AmpliSpeed 热循环仪(Advalytix公司, 德国)。
将志愿者提供的精液和阴道拭子混合制成模拟混合斑, 剪取0.5cm2模拟混合斑样品于1× PBS溶液中, 37℃孵育30min。以13000r/min的转速离心3min, 去上清, 留约20μ L。加入60μ LCarnoy's固定液, 混匀。各取20μ L涂于4张PEN覆膜玻片上(ZEISS公司, 德国), 室温干燥。
玻片置于ThermoBriteTM分子杂交仪上, 56℃烤片2h以上; 将玻片常温下经过0.5mol/L NaOH溶液 4min溶液; 用灭菌水将表面的NaOH冲洗干净, 37℃水浴下玻片经胃蛋白酶溶液(Vysis公司 美国)12min; 后常温下依次经1%甲醛溶液和PBS各5min, 70%乙醇1min。空气中干燥; 选定杂交区域, 加5μ L Vysis CEP®X SpectrumOrangeTMY Spectrum-GreenTM试剂盒中探针杂交液, 盖上盖玻片, 封片, 置杂交仪上73℃变性5min, 39℃孵育6h以上; 去除盖玻片, 74℃水浴下用0.4× SSC洗涤2min, 常温下2× SSC/0.1%NP-40洗涤1min, 避光晾干; 杂交区域加5μ LDAPI复染液, 荧光显微镜下观察结果。
通过PALM激光捕获显微分离系统找到细胞的荧光信号:单个红色为性染色体为X的精子(记为X型精子), 单一绿色信号为性染色体为Y的精子(记为Y型精子); 同时显示两个红色信号为女性上皮细胞。然后, 精子经激光切割弹射到AG480F AmpliGrid(Beckman公司, 美国)收集玻片的各个反应点上。
分别捕获精子细胞10、20、30个, 其中X型精子和Y型精子比例为1∶ 1, 每组重复20次实验。
向每个反应点加入0.75μ L精子裂解液(0.1mg/mL 蛋白酶K(Merck公司, 德国)以及40mmol/L DTT溶液(Solarbio公司, 德国), 用5μ L矿物油(Avalytix公司, 德国)封闭反应体系, 在ASN400E AmpliSpeed 热循环仪上56℃裂解2h, 后99℃变性10min。
在ASN400E AmpliSpeed 热循环仪上应用AmpFlSTRs Identifiler 试剂盒(AB公司, 美国)进行LV-PCR低体积扩增[1, 2, 7]。AmpFLSTR Control DNA 9947A为阳性对照, 选取无荧光信号的区域作为阴性对照。
将每个实验点1.5μ LPCR产物(包括矿物油)全部加入10μ L loading buffer(高纯度甲酰胺(AB公司, 美国)和LIZTM-500(AB公司, 美国)内标的混合物, 混合比例为50∶ 1)中, 然后在3500XL遗传分析仪上进行毛细管电泳。
毛细管电泳数据后, 用Genemapper ID X软件进行数据分析, RFU阈值设为50。将各个反应点STR分型图谱与已知分型结果进行比对, 其中13~16个基因座分型正确为有效分型。
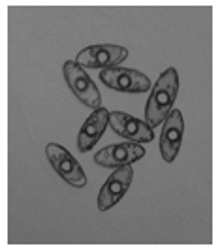
经PALM激光捕获显微分离系统可清晰地观察样本的荧光信号(见图1), 单个红色是性染色体为X的精子, 单一绿色信号是性染色体为Y的精子; 两个红色信号为女性上皮细胞。
样本中的精子以递减的数目各重复20次实验(精子数量为30、20、10), 当精子量为30个时, 20次重复实验有19次得到完整分型。当精子数目降到20或10时, 完整分型的数目对应的降到16和0。等位基因缺失和非特异性扩增数目随着精子数目的减少而增多。20个精子细胞分型电泳图谱见图2。
本课题组前期研究表明:用龙胆紫对精斑进行染色, 既可以清晰辨别精子, 又不影响下游PCR扩增[1]。当检材条件较差时(见图3A), 仅凭形态学难以对细胞进行区分。FISH技术联合PALM激光捕获显微分离系统通过观察不同的荧光信号而使精子细胞的识别更加清晰(见图3B)。
男性精子细胞膜富含二硫键, 较致密, 核内DNA高度凝集。预处理所采用NaOH溶液可以使精子发生去凝集, 使探针和复染液更好的与DNA分子结合, 提高杂交成功率, 增强了染色效果[11]。
实验结果有时会有假阳性出现, 原因有两种可能。一是荧光染料并没有真正进入到细胞中, 而是结合在细胞表面的杂质上; 二是实验人员在操作的过程中口腔上皮细胞脱落, 造成污染。
因为检材中的杂质很多, 荧光探针会非特异性的与之结合, 再加上当检材中精子形态学不完整及数量很少时, 通过荧光显微镜寻找单个红色或绿色荧光信号的精子时费时费力。针对这个问题, 本实验室研究发现, 在观察荧光信号时, 需先使用蓝色荧光时, 如图3B所示, 精子和上皮细胞核的轮廓均清晰可见, 定位后再调至红绿色荧光, 可快速定位细胞的位置。分析原因可能是由于DAPI复染液可穿透细胞膜与核内的DNA结合发挥标记作用, 衬托出细胞的固有形态。对定位后的细胞进行切割弹射过程中, 需首先在弹射点滴加0.6μ L左右的灭菌水, 为细胞提供附着张力。在捕获精子时, 需保证X型精子和Y型精子数相同, 在捕完一类精子时需要在明场下检查(见图4), 确保这类精子数目正确后, 再捕获另一类精子。这样操作时间会延长, 容易使水蒸干, 给实验带来不便。实验中要提高操作的熟练程度, 以加强捕获率。
本研究建立的方法捕获30个精子可获得95%的完整分型, 与常规方法相比灵敏度较高。但与本课题组前期建立的未使用FISH标记的技术方法相比[1], 灵敏度有所下降。分析原因在于, 样本依次经过NaOH溶液、甲醇以及甲醛溶液, 以上物质均有可能造成DNA降解。
鉴于本研究建立的技术方法灵敏度较高, 在实验环境和操作环节都需严格控制污染[12]。本研究中的细胞提取和低体积扩增实验都是在BSL-2生物二级洁净间进行的, 实验室严格分区, 扩增后的产物和收集玻片不能带入细胞提取室。
综上, 荧光原位杂交可清晰地分辨男女性细胞, 便于精细胞的识别, 对于精子形态不规则的检材, 这种方法优势尤为明显。激光捕获显微分离系统可有效分离混合斑中的精子细胞。再联合应用LV-PCR技术, 可成功完成精子的完整分型。因此FISH联用LCM技术为性犯罪案件中混合精斑DNA分型提供了新的思路。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|