作者简介:梅宏成(1984—),男,湖北随州人,汉族,助理研究员,博士,主要从事微量物证检验工作。Tel:13810516746;E-mail:meihongcheng@163.com
目的 建立检验TNT和DNT的双体系胶束电动毛细管色谱方法。方法 在两种不同的胶束电动毛细管色谱缓冲体系下对TNT和DNT进行分离,确定两者在不同体系下的迁移时间Tm值。结果 通过对两者双Tm值的测定,实现了对TNT和DNT准确定性检验。结论 该方法不需大型仪器,操作便捷,可用于实际案件中TNT和DNT的检验鉴定。
Objective To establish a method for detecting TNT and DNT by dual buffer systems Micellar electrokinetic capillary chromatography.Methods TNT and DNT were separated in two different buffer systems by micellar electrokinetic capillary chromatography, and their migration times(Tm) were determined.Results TNT and DNT were qualified accurately through their two migration times(Tm).Conclusion This method is simple, easy operation, and is available for the qualitative detection of TNT and DNT in the actual cases.
毛细管电泳作为一种有效的分离分析技术, 除了具有分析时间短、分辨率高、用样量少等优点外, 同一台仪器还可以根据分析对象选择相应的分离模式[1]。基于这些特点, 毛细管电泳技术被广泛地用于爆炸物和枪弹药及其残留物的分析检验中[2, 3]。毛细管区带电泳利用离子电泳迁移率的不同, 在5min内可以实现无机爆炸残留物中7种最常见无机离子的基线分离[4, 5]。胶束电动毛细管色谱则是在电泳缓冲溶液中加入表面活性剂, 形成动态胶束相, 中性分子可以通过在水相和胶束相之间分配比例的不同而得以分离, 这种方法已被用于有机炸药的分离分析[6, 7]。
然而, 毛细管电泳法也有其局限性。毛细管管壁的不均匀性、缓冲溶液pH的细小变化, 溶液流动对电场的影响均可能造成待分析物迁移时间(Tm)的波动, 降低Tm的重现性, 影响对待测物定性检验的准确性[8, 9, 10]。胶束电动毛细管色谱可以几分钟内完成十几种有机炸药的分离[7], 但其较差的Tm重现性使得该方法很难用于实际案件中未知炸药的定性分析。在本文中, 笔者利用同一毛细管电泳仪可以在多种模式下对待测物进行分离分析的特点, 以TNT和DNT为例, 在两种缓冲体系下对TNT和DNT进行胶束电动毛细管色谱分析, 获得它们的双Tm值, 从而实现了TNT和DNT的准确定性分析, 并将该方法用于实际案例中, 取得了较好的效果。
P/ACE MDQ毛细管电泳仪(贝克曼库尔特公司, 美国), 紫外检测器(固定波长 254nm), 32Karat数据收集与处理软件系统。未涂渍熔融石英毛细管61cm(有效长度53cm)× 75μ m i.d.(河北永年光导纤维厂)。Milli-QⅡ 超纯水装置(美国millipore公司)。
十二烷基硫酸钠(SDS)、乙酸铵、四硼酸钠、甲醇、丙酮均为分析纯。三硝基甲苯(2, 4, 6-Trinitrotoluene, TNT)标准品, 二硝基甲苯(2, 4-Dinitrotoluene, DNT)标准品由中国兵器工业第二〇四研究所提供。所有实验用水均为Milli-QⅡ 超纯水。
缓冲体系Ⅰ (50mmol/L SDS, 50mmol/L乙酸铵):取3.605g SDS, 0.964g乙酸铵溶解定容至250mL容量瓶中, 25℃下保存。
缓冲体系Ⅱ (50mmol/L SDS, 20mmol/L四硼酸钠, 5%甲醇):取3.605g SDS, 1.907g四硼酸钠溶解至250mL容量瓶中, 加入12.5mL甲醇, 混匀定容, 25℃下保存。
TNT和DNT溶液均用甲醇配制成1.0mg/mL, 然后用缓冲溶液稀释成0.01mg/mL, 4℃下保存备用。两者的混合溶液也用甲醇配制, 含TNT和DNT各1.0mg/mL, 然后用缓冲溶液稀释成0.01mg/mL, 4℃下保存备用。
所用缓冲溶液在实验前先超声脱气10min。毛细管初次使用时依次用0.5mol/L氢氧化钠、超纯水各清洗10min, 再用缓冲溶液平衡20min。采用压力进样法, 压力为0.5psi, 进样时间为5.0s。分离电压为30kV。实验温度为25℃。所有样品均分别在缓冲体系Ⅰ 和缓冲体系Ⅱ 条件进行分离分析。
实际案例中的检材先用丙酮提取至一烧杯, 挥干丙酮, 加入0.5mL甲醇, 充分振荡后取0.1mL甲醇溶液, 用缓冲溶液稀释至1.0mL, 所得溶液分别在两种缓冲体系下进行胶束电动毛细管色谱法分析。
目前国内外对胶束电动毛细管色谱分析有机炸药进行了很多研究, 利用该方法可以在几分钟里实现十几种, 甚至几十种有机炸药的分离分析[7]。然而, 在实际操作中发现, 这种方法分析有机炸药的重现性并不是很理想, 特别是对于操作经验不是很丰富的检验人员来说, 不同时间分析同一样品所得的迁移时间可能差别会很大, 难以对有机炸药进行准确认定。
为了解决这个问题, 本实验利用毛细管电泳仪很容易变换分离模式的特点, 选择在两种不同的缓冲体系中对有机炸药进行胶束电动毛细管色谱分析。同一种有机炸药在不同的缓冲体系中在水相和胶体相中分配比例不同, 导致迁移时间发生改变, 因此其在两个不同的缓冲体系中具有不同的特征迁移时间(Tm)。如果某一物质在两种缓冲体系中的Tm值和已知有机炸药的Tm的偏差均小于5%, 那么就可以确定该物质即为已知有机炸药。
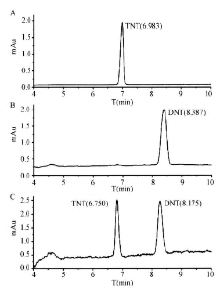
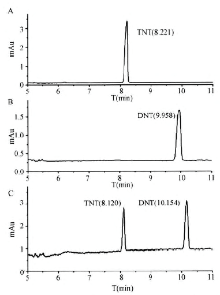
以TNT和DNT为例, 笔者考察了胶束电动毛细管色谱法在两种不同缓冲体系下对它们的分离情况。分别在缓冲体系Ⅰ (50mmol/L SDS, 50mmol/L乙酸铵)和缓冲体系Ⅱ (50mmol/L SDS, 20mM四硼酸钠, 5%甲醇)的条件下对0.01mg/mL TNT, 0.01mg/mL DNT, 0.01mg/mL TNT和DNT混合溶液进行胶束电动毛细管色谱分析, 分离电压为30kV(见图1, 图2)。
从图1可以看出, 在缓冲体系Ⅰ 中TNT的Tm为6.983, 相对于混合溶液中TNT的Tm为6.750的相对偏差是3.5%, DNT的Tm为8.387, 相对于混合溶液中DNT的Tm为8.175的相对偏差是2.6%; 从图2可以看出, 在缓冲体系Ⅱ 中TNT的Tm为8.221, 相对于混合溶液中TNT 的Tm为8.120的相对偏差是1.2%, DNT的Tm为9.958, 相对于混合溶液中DNT的Tm为10.154的相对偏差是1.9%。TNT和DNT在两种缓冲体系中的迁移时间相对于其在混合溶液中的迁移时间的相对偏差均小于5%, 因此可以用这种方法对TNT和DNT进行定性分析。
利用上面所建立的双体系胶束电动毛细管色谱法, 对某年10月在内蒙古某地发生的一起爆炸案件中的检材进行了炸药残留物分析。通过该方法的检验, 在现场提取的铁管内检出梯恩梯成分, 这一结论与HPLC/MS/MS检验的结果一致, 表明该方法可用于实际爆炸案件中有机炸药的定性分析检验。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|