作者简介:郝红霞(1976— ),女,内蒙古人,博士,主要从事毒物分析工作。Tel:010-68645052;E-mail:haohx@126.com
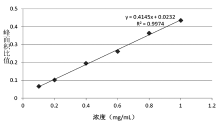
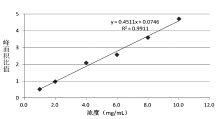
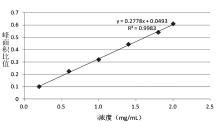
目的 建立气相色谱同时测定血清中甲醇、乙醇、正丙醇含量的方法。方法 改变气相色谱条件,以异戊醇为内标,采用气相色谱-氢火焰离子化检测器对血清直接进行检测。并通过待测组分与内标物的响应值比进行定量。结果 GC/FID法检测血清中的甲醇、乙醇、正丙醇含量,得到了良好的线性关系。乙醇浓度从1~100mg/100mL的线性关系式为Y=0.4145X+0.0232(R2=0.9974)、浓度从100~1000mg/100mL的线性关系式为Y=0.4511X+0.0746(R2=0.9911),甲醇浓度从1~200mg/100mL的线性关系式为Y=0.2778X+0.0493(R2=0.9983)。结论 该方法操作简便快速,重现性好,通过检测正丙醇还可以推断腐败血样自身产生的乙醇量,是一种较为理想的血醇检测方法。
Objective To develop a method for simultaneous determination of methanol, ethanol and propanol in blood by Gas Chromatography.Methods Conditions of gas chromatography were optimized and then blood serum samples were analyzed quantitatively by GC/FID.Results Linear relations of ethanol were Y=0.4145X+ 0.0232(R2=0.9974)for the concentration ranged from 1 to 100mg/100mL and Y=0.4511X+0.0746(R2=0.9911)for the concentration ranged from 100 to 1000mg/100mL. Linear relation of methanol was Y=0.2778x+0.0493(R2=0.9983)for the concentration ranged from 1 to 200mg/100mL.Conclusion This method can be applied in clinical diagnosis of poisoning and forensic analysis of alcohol in blood.
乙醇(分子式C2H6O)俗称酒精, 是酒的主要成分, 乙醇进入空胃后, 可于30min~90min内在胃及肠道内被完全吸收入血, 15min~90min内, 血液中酒精浓度值( blood alcohol concentration, BAC )可达到峰值[ 1 ] 。其代谢主要是在肝脏内被氧化分解, 少部分以原形经呼吸道、尿、汗直接排出体外。过量饮用含酒精类饮料不仅可引起心脑血管、消化、神经系统等多种病症, 还可致驾驶员酒后动作失常、判断思维能力下降, 成为诱发道路交通事故的主要原因之一。据相关部门统计2001年中国酒后驾车造成的死亡人数占到了道路交通事故总死亡人数的30%以上[ 2 ] 。以BAC值作为酒后驾驶和醉酒程度的判定依据, 已广泛为交警等执法部门采用并被多个省市纳入道路安全地方性标准。早期由于科技不发达, 采用的多是化学法[2, 3]进行检测, 随之迅猛发展的是气相色谱法, 有顶空气相色谱法[4, 5, 6], 标准曲线色谱法[7, 8, 9], 直接进样色谱法[10, 11, 12], 酶检测法[13, 14, 15, 16], 分析仪器检测法[17, 18, 19]等。本文建立的气相色谱同时测定血清中甲醇、乙醇、正丙醇含量的方法, 是一种较为理想的血醇检测方法, 报道如下。
TP2100气相色谱仪, 配有火焰离子化检测器和色谱数据工作站。
空白抗凝血, 甲醇、乙醇、正丙醇、异戊醇(内标)储备液配制, 所用标准均为优级纯, 采用重蒸馏水或去离子水。
色谱柱:DM-WAX30m× 0.25mm× 0.25μ m弹性石英毛细柱。
进样口温200℃, 检测器温FID 220℃, 柱温95℃(5min)→ 5℃/min→ 110℃(0min)→ 30℃/min→ 220℃(0.5~1min), 载气高纯N299.999。
柱流速1mL/min, 恒压, 分流比10:1, 尾吹气 29mL/min; H2 30mL/min; 空气 300mL/min。
用移液器分别准确吸取无水甲醇1.26mL、(相对密度0.7913)无水乙醇1.26mL(相对密度0.7893)、正丙醇1.240mL(相对密度0.8037)于50mL容量瓶中, 异戊醇1.230mL(相对密度0.8110)于250mL容量瓶中, 用重蒸水稀释至刻度, 混匀, 分别得浓度为20.0mg/mL的甲醇、乙醇、正丙醇标准储备液, 4.0mg/mL异戊醇标准储备液, 置4℃冰箱保存(可保存1年)。
1.5.1 甲醇、乙醇、正丙醇混标液 准确吸取甲醇储液1.00mL, 乙醇储液1.00mL, 正丙醇储液0.50mL同于10mL容量瓶中, 加去离子水至刻度混匀, 即得甲醇2.0mg、乙醇2.0mg、正丙醇1.0mg/mL混合标准溶液。使用期3个月。临用时将该混标液按比例稀释10倍后, 得浓度甲醇0.2mg、乙醇0.2mg、正丙醇0.1mg/mL混标液, 供仪器的定性分析用。
1.5.2 含内标异戊醇的醇混标液 准确吸取4.0mg/mL异戊醇储备液1.0mL于10mL容量瓶中, 加去离子水至刻度, 混匀后得0.4mg/mL异戊醇内标液(使用期1个月)。准确吸取甲醇0.2mg、乙醇0.2mg、正丙醇0.1mg/mL混标液200μ L, 加0.4mg/mL。异戊醇内标液800μ L混匀获得。本混标液供考查仪器的稳定性和灵敏度使用, 临用时配制。
1.6.1 甲醇0.2~2.0mg/mL和乙醇0.1~1.0mg/mL混合标准系列 (1)甲醇、乙醇单一标准液:准确量取甲醇、乙醇储备液一定量, 用去离子水稀释后获得甲醇4.0mg/mL和乙醇2.0mg/mL的备单标液。
(2)混标系列配制:取5mL的容量瓶6个, 从低浓度到高浓度编号后备用。分别吸甲醇4.0mg/mL和乙醇2.0mg/mL单标液各一定量于系列容量瓶中, 最后用去离子水至刻度混匀后备用, 各系列浓度所需甲醇、乙醇单标液体积见表1。
(3)0.4mg/mL异戊醇内标液:取4.0mg/mL异戊醇储备液一定量稀释10倍获得, 临用时稀释。
| 表1 甲醇、乙醇混标系列 |
(4)各标准系列仪器分析试样制备:准确吸取各标准系列200μ L, 加0.4mg/mL异戊醇内标液800μ L混匀, 备检做标准曲线。
1.6.2 乙醇1~10mg/mL和正丙醇0.8~4mg/mL混标系列 (1)乙醇和正丙醇单标液准备:直接用20mg/mL乙醇单标储备液和20mg/mL正丙醇单标储备液配制。
(2)混标系列配制:取5mL的容量瓶6个, 从低浓度到高浓度编号后备用。分别取乙醇20mg/mL和正丙醇20mg/mL单标储备液一定量于系列容量瓶中, 最后加去离子水至刻度混匀后备用。各系列浓度所用乙醇和正丙醇单标液见表2。
| 表2 乙醇、正丙醇混标系列 |
(3)0.4mg/mL异戊醇内标液:配制方法见1.6.1。
(4)各标准系列仪器分析试样制备:准确吸取各标准系列200μ L, 加0.4mg/mL异戊醇内标液800μ L混匀, 备标作标准曲线。
1.7.1 检血 取送检血样1~2mL, 于3000r/min下离心5min, 上清液备用。
1.7.2 配样 准确吸取检血离心5min后的上清液200μ L于1~2mL的试管中, 加0.4mg/mL异戊醇内标液800μ L, 混匀后供仪器分析。每一个检材必须配制2~3份试样, 求各试样的定量数据的平均值作为检材的定量值。
1.7.3 空白血添加乙醇试样的制备 取加过抗凝剂的空白血4.0mL, 加入20mg/mL乙醇储备液1.0mL, 轻摇混匀30min以上得血中乙醇浓度4.0mg/mL添加标准血样。取该血样一定量配制成0.20, 0.50, 0.80mg/mL乙醇浓度血样。
取上述0.2, 0.5, 0.8mg/mL乙醇浓度血样于3000r/min离心5min, 上清液取200μ L, 加入800μ L(0.4mg/mL)异戊醇内标液混匀供仪器分析, 以准确定量检材中乙醇用量。添加血试样必须做2份以上重复, 以保证定量数稳定。
设定乙醇优化后的分析条件, 待仪器处在Ready状态时, 连续进样乙醇0.2mg、甲醇0.2mg、正丙醇0.1mg/mL混标液, 考查仪器灵敏度状态和稳定性, 一般进行3~4次重复考量。之后再以乙醇0.5mg、甲醇0.5mg、正丙醇0.2mg/mL混标液200μ L, 加入800μ L 0.4mg/mL异戊醇内标液混匀制成的试样, 进样3~4次, 依各醇与内标的峰面积比值是否一致考查仪器的稳定状态。
当仪器处于优化后的最佳状态时, 将配制好的标准系列依次分析, 每次进样1μ L, 每个试样进样2~3次, 以甲醇、乙醇、正丙醇各自浓度下的峰面积与内标峰面积比值的平均值为纵坐标, 以绘制该醇的浓度为横坐标, 绘制各定量醇的标准曲线。
2.3.1 定性和粗定量 仪器在优化稳定状态, 取检血试样1μ L进样, 每个试样进样2~3次。计算检血中可疑组分的Rt值平均值, 与标准的Rt值作比较, 以Rt值的一致性定性。求出检血中乙醇与内标物异戊醇的峰面积比值平均值, 查曲线计算出检血中乙醇的浓度。其他甲醇或正丙醇含量依次类推。
2.3.2 准确定量 根据查标准曲线获得的检血中乙醇的浓度, 配制相应浓度的添加血样后制成仪器分析试样, 再经仪器分析、统计, 计算得出检血中乙醇的标准定量数据。
2.3.3 定量计算公式 W乙醇=A检/A添× C标, 式中:W乙醇为检血中乙醇的浓度(mg/mL), A检指检血中乙醇与内标异戊醇的峰面积比值, A添指空白添加血中乙醇与内标异戊醇的峰面积比值, C标为空白添加血中乙醇的浓度(mg/mL)。
相对相差计算公式如下:
式中:C1、C2为两份检材平行定量结果, C为两份检材平行定量结果的平均值, 即:
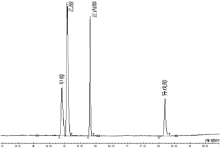
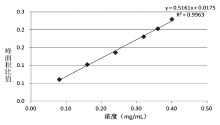
各标准的保留时间参考值及定量曲线见表3及图1~图4。乙醇的定量限为0.10mg/mL。
| 表3 各醇在GC/FID上的Rt值 |
3.2.1 定性 (1)检血中未见乙醇或甲醇的色谱峰, 而见内标物的色谱峰, 而且内标物的色谱峰的峰面积值与往常相近, 说明仪器状态正常, 可判定检血中不含甲醇或乙醇成分。(2)以异戊醇为内标, 计算色谱峰的相对保留时间, 与乙醇或甲醇对内标物异戊醇的相对保留时间比较, 误差小于2%时, 可以确定检材中含乙醇或甲醇; 大于2%时不可认定。(3)如果检血试样中未出现内标物色谱峰或峰面积值不近似于往常, 检验结果无效, 应检查原因, 重新检验。(4)本方法检测血液中检出限:甲醇、乙醇均为0.05mg/mL, 检材中乙醇含量低于10mg/100mL时, 建议不给出定性定量数据, 检验结果判为阴性。
3.2.2 定量 (1)检材血应平行制样, 测2份以上, 2份检材试样定量数据的相对相差不得超过10%, 定量结果的报出以2份试样定量数据平均值为准。超过10%相对相差的定量结果不准确, 需重新定量。
(2)本方法采用血样直接进样方法检验甲醇和乙醇, 因此, 必须考虑送检血样是否加抗凝剂。加入抗凝剂的检材血样可以直接报告定量结果。未加抗凝剂的检血样定量结果代表着检血中血清中的血醇浓度, 不能代表全血的浓度。根据人体中血清占全血的比例约在60%左右, 因此报出血醇定量结果应在定量数据上乘以80%的系数, 使血醇的浓度更加接近全血浓度。
(1)血液腐败可生成乙醇, 因此在测定腐败血时注意:腐败血生成乙醇的同时, 也平行的生成正丙醇, 因此检血中检出乙醇, 而未检出正丙醇者, 此时检出的乙醇可以认为非血液腐败产生的乙醇。
(2)腐败血液中检出乙醇的同时, 也检出正丙醇, 此时对血液中乙醇含量评判为:第一, 血液中乙醇的含量在正丙醇含量的20倍以下, 此时应考虑为血中乙醇由腐败而产生, 判为阴性。第二, 血中乙醇的含量高于正丙醇含量20倍以上, 此时则认为血中乙醇由血液腐败和非血液腐败两部分组成, 非血液腐败的乙醇含量计算, 可将检出乙醇的浓度值减去相当20倍正丙醇浓度的乙醇浓度值, 余下值则是血中乙醇浓度的下限值。
中国交通法规给出20mg/mL酒后驾车和80mg/mL醉酒驾车的评判阈值。因此当定量结果血中浓度为0.2mg/mL和0.8mg/mL附近值时, 必须给出定量结果的不确定度值。所以, 在收到检测血醇含量的检材后应立即实施检验, 以保证血中乙醇含量检测的真实性。
本实验室已经连续两年参加酒精的实验室能力验证活动, 均取得满意的评价。能力验证(Proficiency Testing)是利用实验室间比对来判定实验室和检查机构能力的活动, 也是认可机构加入和维持国际相互承认协议(MRA)的必要条件之一。以2011年为例, 能力验证提供方提供两个待测血样, 要求对血液中的乙醇含量进行检测。依照上述方法, 本实验室就两个待测组分进行检测, 并监控正丙醇的含量, 以确保精确的测量乙醇, 得到验证方的反馈结果见表4:
| 表4 实验室能力验证结果评价 |
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|