作者简介:曾宪海(1979—),男,湖北谷城人,主检法医师,博士,主要从事法医DNA检验鉴定和法医遗传学研究。E-mail:xhzengwh@163.com
目的 建立减少DNA低体积扩增过程中产生气泡的方法。方法 采用激光显微切割技术、PALM系统收集目标细胞,并在1μL~1.5μL低体积扩增样本,加入扩增液0.7μL~0.8μL。结果 低体积扩增反应中的失败位点比例为2.3%,比常规反应位点时常会产生气泡导致该位点样本扩增失败且达30%以上的比例显著降低。结论 低体积扩增方法可以减少或克服扩增过程中气泡的产生,提高扩增成功率。
Objective To establish a new method for reducing the bubbles in process of Low Volume PCR (LV-PCR).Methods Target cells were collected under Laser Capture Microscope and LV-PCR was performed.Results Bubbles can be reduced by skillful collection operations and LV-PCR amplification.Conclusion The LV-PCR method was better than standard PCR method for analysis of varying concentration DNA samples.
微量混合生物物证常规方法检验所得到的混合图谱, 由于其不能达到认定的作用而使其价值偏低。这类检材经过复杂的方法提取, 得到的DNA量少、浓度低、抑制物多, 使用常规方法扩增, 电泳后所获得的图谱峰值低、杂峰多、易丢带[1, 2, 3, 4, 5]。激光显微切割技术(利用PALM系统进行细胞收集) 能从混合样本中收集到单一的目标细胞, 低体积扩增技术能利用极少量细胞得到纯净图谱, 二者的联合应用能够解决以上问题, 具有重大的发展潜力。然而, 在低体积扩增技术转化应用的实验过程中, 反应位点时常会产生气泡导致该位点样本扩增失败且达30%以上比例, 使这种方法应用性不强。为克服这一不利因素, 笔者从实验方法上梳理, 以图减少低体积扩增中气泡的产生, 使该技术有更大的应用价值。同时, 采用陈旧的案件样本, 在不同样本浓度条件下, 通过比对扩增产物的图谱来比较低体积扩增方法与常规扩增方法的差别, 进而确定其是否具有解决以上问题的应用价值。
样本一:棉签或水瓶上的口腔上皮细胞, 用于单细胞捕获。
样本二:日常案件的4个检材, 常规Chelex-100法方法提取, 4℃放置一个月, 将每个样本按原浓度的1、1/2、1/4和1/8倍稀释, 用于两种扩增方法的比较。本实验用的4个样本是日常案件检验的存留物, 存在较多的抑制物, 相对于纯净的9947A, 更接近于法医实战检验, 用其进行实验, 能较好的体现两种扩增技术在法医检案应用中的差异。
PALM系统(ZESS), PEN1.0 玻片, AG480F AmpliGrid反应玻片及密封油, 0.04mol/L PK溶液, Identifiler试剂盒(AB公司), GeneAmp 9700 PCR扩增仪, AmpliSpeed ASN400 PCR扩增仪, ABI-3130XL遗传分析仪。
1.3.1 激光显微切割技术的构建 用PALM系统收集目标细胞及扩增样本制备。
洗脱:将带有目标细胞的棉签放入有700μ L去离子水的EP管内, 震荡洗脱5min, 取出棉签, 13000r/min离心3min, 吸去上清液, 保留约30μ L, 加入适量的染料, 混匀供试验用。在洗脱目标细胞过程中, 尽可能的减少会影响涂片的均匀度的载体进入洗脱液(如, 较大颗粒或纤维), 染色时染色剂要离心, 避免带入染色剂颗粒, 影响制片。
制片:制片过程包括涂片与烘干, 加入约5μ L的洗脱液在PEN 1.0 玻片上, 用枪头与其呈0角度轻轻涂抹, 以不划伤PEN 1.0 玻片的膜为宜。用热块37℃烘干, 或在GeneAmp9700扩增仪上, 37℃烘干10min~15min左右。
切割:利用PALM系统(Zess)的显微镜进行观察选择结构清晰、周围比较干净的单个细胞, 用绘制工具标记目标细胞, 使用其激光系统对目标细胞所附着的PEN 1.0玻片膜切割。切割的激光束能量要适中, 通常以切割下来的PEN 1.0 玻片膜膜面在视野中稍变模糊为宜。
收集与消化:细胞收集时直接加PK溶液0.7μ L~0.8μ L到AG480F AmpliGrid玻片反应位点, 用PALM系统的查找功能快速收集, 在消化液未干前完成收集, 此时如果消化液比较少, 以空白对照的体积为依据, 加适量的消化液或者去离子水, 然后用约5μ L油密封, 不要导入气泡。油封闭后静置5min~10min, 待反应液体沉到AmpliGrid反应玻片上后, 56℃消化1h, 95℃变性15min。
扩增液添加:加入扩增液(Identifiler试剂盒, 配比为:Mix4.2, Primer2.3, Golden酶0.5)0.7μ L~0.8μ L。添加时尽量使用小枪头, 让其在枪头尖上形成小液滴, 然后轻微接触密封油膜顶端, 让其自行融入样本溶液即可。静置一会, 检查每个扩增点顶端是否被油膜重新封住, 如果没有加少量的密封油, 可避免扩增过程中出现吹气泡的现象。
1.3.2 两种扩增方法比较 将准备好的样品分别用常规方法(GeneAmp 9700 PCR扩增仪, 10μ L 体系, 按Identifier 试剂盒说明操作)和低体积扩增方法(AmpliSpeed ASN400 PCR扩增仪)扩增。后者的扩增体系样本为1μ L~1.5μ L, 先在AG480F AmpliGrid反应玻片上加入0.75μ L的样品, 用油封闭, 再按以上扩增液添加方法加入扩增混合液0.75μ L, 静置5min后启动反应。反应过程为95℃变性11min, 28个扩增循环, 60℃下延伸1h。两种方法获得的PCR产物同时上样, 经ABI -3130XL遗传分析仪检测, GeneMapper ID v3.2分析检测结果。
经以上各操作步骤的优化, 在后续低体积扩增反应中的失败位点比例为2.3%(132个位点, 失败3个, 其中2位点由于变性过程升温过快, 油膜破裂与附近一个位点融合)。
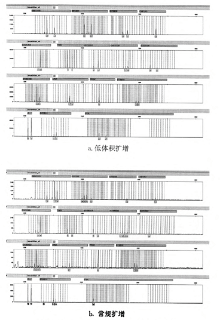
低体积扩增产物的检验峰值(均值在4000左右)高于常规方法扩增产物(均值在2000以下, 见图1), 二者间峰值的差别在稀释2倍和4倍时最大。在分型成功率上, 低体积扩增方法能够获得更为准确的结果且成功率明显高于常规扩增方法; 在丢失位点数量上, 二者差别不大; 在峰带丢失数量上, 常规方法明显高于低体积扩增方法且主要体现在稀释倍数较高的样本, 如稀释4倍和8倍样本(见表1), 常规方法峰值低, 较大的片段不能或不能完全检验出信号, 如图1b中, 常规体积扩增在D2S1338和FGA位点上丢带。
在图谱判读上, 同一个位点出现多个差别不大的峰值是引起误判甚至是无法判读的主要原因之一(如图1b中在位点D8S1179、D21S11、D16S539和D5S818位点)。这样的位点在常规扩增方法中明显多于低体积扩增方法(见表1)。本实验中常规方法出现的多个峰与真实峰之间没有相关性。
| 表1 常规扩增方法和低体积扩增方法对同一样品(N=4)在不同浓度下主要参数比较(Identifiler, AB公司) |
在DNA提取方法上大量改进以提高检验的质量[6, 7, 8, 9, 10, 11, 12]是法医工作者一直以来致力的研究方向之一, 激光显微切割技术与众多提取技术一样具有广泛的应用价值[13, 14, 15]。激光显微切割与低体积扩增联合应用技术的价值体现在, 能从微量混合样本中收集单一种类的细胞并检验出单一样本的结果, 对案件的认定意义重大。这项技术联合应用中, 低体积扩增技术的升温过程是一个对密封液体快速加热的过程, 密封液内如存在微小气泡, 会因此产生气溶胶, 气溶胶的聚集会形成气泡, 导致扩增失败。本文构建的激光显微切割技术操作步骤, 目的是在前期的细胞提取操作过程中, 减少或者消除微小气泡被带入到密封液内, 从而减少低体积扩增过程中气泡的产生, 提高扩增成功率, 本文的研究也表明这种方法效果明显。
相对于常规扩增体系, 低体积扩增体系的体积由10μ L缩减到1μ L, 节省了试剂, 半球状的密封空间提供了最佳微反应环境, 提高了反应灵敏度[16]。本实验的两种扩增方法检验结果显现的差异也表明低体积扩增方法具有显著优势。相对于常规扩增方法, 低体积扩增体系体积小, 提高了样本在扩增体系中的浓度, 这与低体积扩增产物图谱的峰值普遍高于常规体积扩增方法有关; 另外, 引物结合时间和延伸时间延长可能也与此结果有关。对于陈旧样本, 低体积扩增方法能克服用常规方法所不能克服的在某些位点容易出现两个以上峰值的情况, 这也是这种低体积扩增方法的一个重要优势。低体积扩增方法的另一个优势体现在对低浓度样本的高灵敏度上。随着样本浓度的降低, 低体积扩增方法获得的图谱峰值没有变化, 而常规扩增方法图谱的峰值明显下降, 同时低体积扩增方法获得的图谱丢失峰带和引起误判位点减少的现象, 相对于常规方法在这二个参数上的增加也表明了其优势。
综上所述, 本文的研究结果表明, 在激光显微切割技术与低体积扩增技术结合应用的过程中, 通过操作方法的改进, 可以减少微小气泡被带入收集样本中, 进而减少或克服低体积扩增过程中的气泡产生, 提高扩增成功率。同时通过与常规扩增方法的比较, 低体积扩增方法对陈旧的、浓度低的、抑制物较多的样本, 在检出质量上具有较明显的优势。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|